
I prodotti combinati, ovvero prodotti che uniscono medicinali, dispositivi o biologici, presentano problemi speciali di etichettatura normativa. Poiché questi prodotti sono costituiti da più componenti e standard normativi variabili, i produttori devono assicurarsi di rispettare tutti i requisiti individuali e di trasmettere correttamente le informazioni sulla sicurezza.
Questo blog esplora le sfide dell'etichettatura dei prodotti combinati e fornisce strategie per orientarsi tra i requisiti normativi di etichettatura, dando priorità alla sicurezza e alla conformità del paziente. La Figura 1 evidenzia le principali sfide legate all'etichettatura dei prodotti combinati.
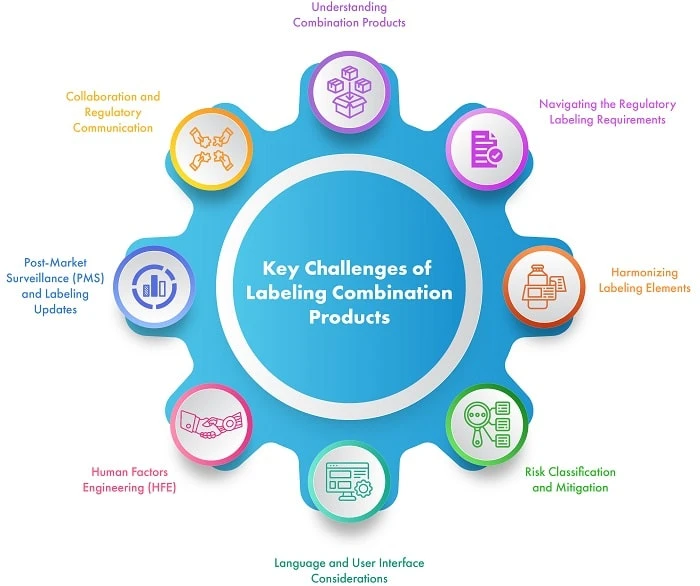
Figura 1: Sfide principali dell'etichettatura dei prodotti combinati
Esaminiamo us ciascuna sfida nel dettaglio:
- Capire i prodotti combinati: I prodotti combinati combinano vari componenti, ad esempio un prodotto composto da un farmaco e un dispositivo, per offrire scelte terapeutiche innovative. Tuttavia, la convergenza di diversi quadri normativi e requisiti può complicare il processo di etichettatura. È quindi fondamentale riconoscere il metodo di funzionamento fondamentale e le normative pertinenti per ciascun componente.
- Orientarsi nei requisiti normativi di etichettatura: I prodotti combinati devono rispettare sia le leggi sui farmaci che quelle sui dispositivi, rendendo necessario orientarsi tra molteplici percorsi normativi. Collaborare strettamente con esperti di Affari Regolatori per comprendere e affrontare i requisiti specifici di etichettatura stabiliti da agenzie come la United States Food and Drug Administration (USFDA), l'European Medicines Agency (EMA) e altre autorità competenti.
- Armonizzazione degli elementi di etichettatura: L'armonizzazione degli elementi di etichettatura tra i diversi componenti dei prodotti combinati è fondamentale per fornire informazioni chiare e coerenti agli operatori sanitari e ai pazienti. Assicurarsi che l'etichettatura rappresenti accuratamente la funzionalità combinata e trasmetta istruzioni, avvertenze e istruzioni per l'uso (IFU) essenziali.
- Classificazione e mitigazione dei rischi: Identificare e classificare i rischi associati a ciascun componente del prodotto combinato. Valutare i rischi potenziali e determinare le strategie di mitigazione appropriate. Comunicare questi rischi, insieme alle precauzioni e alle avvertenze corrispondenti sull'etichetta del prodotto, per garantire la sicurezza del paziente e l'aderenza ai requisiti di etichettatura previsti dalla normativa.
- Considerazioni sulla lingua e sull'interfaccia utente: Considerare i requisiti linguistici per l'etichettatura quando si commercializzano prodotti combinati a livello internazionale. Tradurre e localizzare i contenuti dell'etichettatura per essere conformi alle normative delle diverse regioni e per soddisfare le preferenze linguistiche del pubblico di destinazione. Inoltre, è necessario progettare interfacce di facile utilizzo che facilitino l'uso sicuro ed efficace dei prodotti combinati.
- Ingegneria dei fattori umani (HFE): L'usabilità dei prodotti combinati è fondamentale per garantire la sicurezza del paziente. Applicare i principi HFE per garantire che l'etichettatura e le istruzioni per l'uso siano intuitive, facilmente comprensibili e compatibili con l'interfaccia utente del componente del dispositivo. Effettuare test di usabilità e iterare la progettazione per ridurre il rischio di errori e ottimizzare l'esperienza dell'utente.
- Post-market Surveillance (PMS) e aggiornamenti dell'etichettatura: Monitorare continuamente la sicurezza e le prestazioni dei prodotti combinati tramite Post-market Surveillance (PMS). Acquisire e analizzare tempestivamente gli eventi avversi e le nuove preoccupazioni relative alla sicurezza. Aggiornare l'etichettatura, se e quando necessario, per riflettere nuove informazioni, avvertenze di sicurezza o modifiche nelle indicazioni.
- Collaborazione e comunicazione normativa: L'etichettatura dei prodotti combinati richiede una stretta collaborazione tra i team di regolamentazione, qualità e marketing. Stabilire canali di comunicazione efficaci con le autorità regolatorie per ottenere indicazioni, chiarire i requisiti e garantire la conformità durante l'intero processo di etichettatura. Sfruttate le competenze dei team interfunzionali per sviluppare un'etichettatura completa e conforme.
Conclusione
Il Labelling dei prodotti combinati implica la navigazione di complessi quadri normativi, l'affrontare la classificazione del rischio e l'assicurare una comunicazione efficace delle informazioni di sicurezza. Comprendendo le sfide uniche, armonizzando gli elementi di Labelling e sfruttando l'esperienza normativa, i produttori possono gestire le sfide con facilità e dare priorità alla conformità e alla sicurezza del paziente.
Presta particolare attenzione ai requisiti normativi ed etichetta accuratamente i tuoi prodotti combinati, consentendo agli operatori sanitari e ai pazienti di utilizzarli in modo sicuro ed efficace. Collaborare con un esperto come Freyr ridurre al minimo i tuoi sforzi. Contattuseci per saperne di più!









