Nel panorama in continua evoluzione dello sviluppo farmaceutico, il percorso dalla scoperta in laboratorio al trattamento del paziente è costellato di complesse sfide normative. In questo processo si trova la New Drug Application (NDA), una pietra miliare critica che comprende impegno scientifico e investimento. Questo blog approfondisce le complessità delle operazioni normative NDA, offrendo preziosi spunti e lezioni apprese da veterani del settore.
Il panorama NDA
Le domande di autorizzazione per nuovi farmaci rappresentano il culmine di un'ampia ricerca, sviluppo e test clinici. Servono come dossier completo che convince le autorità regolatorie, come la U.S. Food and Drug Administration (FDA), che un nuovo farmaco è sicuro, efficace e pronto per l'approvazione all'immissione sul mercato.
La Complessità del Processo NDA
Uno dei principali ostacoli nelle presentazioni NDA è l'enorme volume e la complessità dei dati richiesti. Le aziende farmaceutiche devono districarsi in un labirinto di linee guida normative, presentando al contempo prove chiare e convincenti dei meriti del loro prodotto farmaceutico. Questo atto di bilanciamento spesso porta a ritardi, revisioni costose e, in alcuni casi, a rifiuti totali.
Per far luce su questo processo critico, analizziamo le fasi chiave della presentazione di una NDA ed esploriamo le strategie per il successo in ogni fase.
Tabella 1: Fasi chiave nella presentazione di una NDA
| Palcoscenico | Descrizione | Migliori pratiche |
|---|---|---|
| Ricerca preclinica | Studi di laboratorio e su animali per raccogliere i dati iniziali | Garantire una progettazione solida dello studio e una raccolta meticolosa dei dati. |
| Sperimentazioni cliniche | Sperimentazioni umane condotte in fasi (I, II, III) | Implementare protocolli rigorosi e mantenere l'integrità dei dati |
| Documentazione | Raccolta di dati di sicurezza, efficacia e qualità | Organizzare i dati in modo sistematico e garantire la chiarezza della presentazione. |
| Revisione normativa | Presentazione alla FDA e processo di revisione | Mantenere una comunicazione aperta con gli enti normativi |
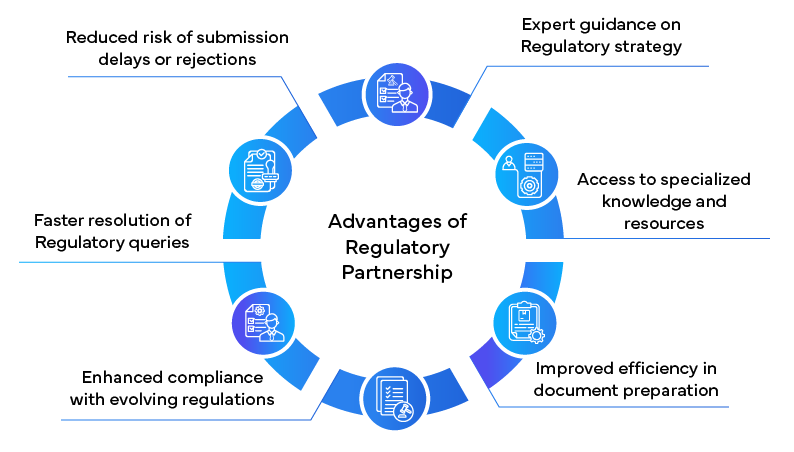
Ruolo del partenariato normativo
Nel navigare il complesso panorama delle NDA, molte aziende farmaceutiche si rivolgono a partner normativi per supporto. Queste aziende specializzate offrono una vasta esperienza e competenza che possono semplificare significativamente il processo di NDA.
Lezioni apprese
Guardando al futuro, l'importanza di operazioni Regolatorie NDA efficaci non farà che aumentare. Con il ritmo dell'innovazione in accelerazione e i contesti Regolatori in evoluzione, coloro che padroneggeranno questo processo cruciale saranno nella posizione migliore per portare trattamenti che cambiano la vita ai pazienti di tutto il mondo.
Il percorso per una presentazione NDA di successo è raramente semplice; inoltre, adottando un approccio strategico alle operazioni normative, sfruttando partnership con esperti e mantenendo un impegno per la qualità e la conformità, le aziende farmaceutiche possono migliorare significativamente le loro possibilità di successo della NDA.