L'artwork di imballaggio è più di una semplice progettazione, è un requisito di conformità obbligatorio per la presentazione all'autorità sanitaria e anche per la commercializzazione dell'imballaggio. All'interno dell'Unione Europea (UE), i prodotti farmaceutici devono aderire ai requisiti centralizzati dell'artwork stabiliti dalla Direttiva 2001/83/CE. Tuttavia, molti Member States dell'UE applicano anche requisiti locali aggiuntivi basati sulla lingua, sulle leggi nazionali e sull'accessibilità per i pazienti per i loro imballaggi primari e secondari.
La comprensione di queste sfumature è fondamentale per le aziende farmaceutiche che intendono garantire la conformità normativa, evitare costosi ritardi e semplificare l'ingresso sul mercato.
Requisiti di Artwork a livello UE: Le basi
Ai sensi dell'articolo 54 della direttiva 2001/83/CE, tutti i medicinali per uso umano devono riportare le seguenti informazioni sull'imballaggio esterno e interno:
- Nome del medicinale (compreso il dosaggio e la forma farmaceutica)
- Principi attivi e quantità
- Via di somministrazione
- Data di scadenza
- Istruzioni per la conservazione (se applicabile)
- Avvertenze speciali (se necessario)
- Numero di lotto
- Dettagli del produttore
- Braille il nome del medicinale
Questi sono obbligatori in tutti i Paesi dell'UE e garantiscono una base coerente per la sicurezza dei pazienti e la chiarezza delle informazioni.
Requisiti specifici per l'Artwork per paese
Nonostante le normative armonizzate dell'UE, i singoli paesi applicano condizioni specifiche per l'Artwork e l'etichettatura. Ecco una panoramica dei requisiti chiave specifici per paese:
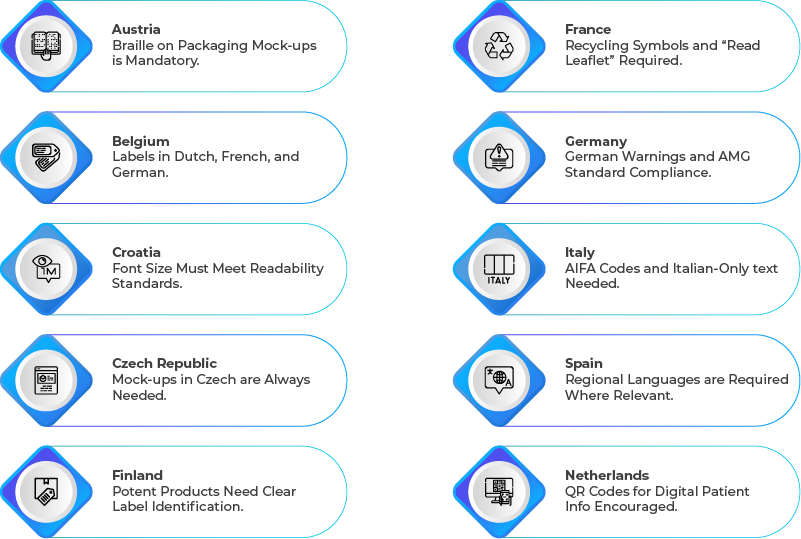
Perché la conformità varia
Ogni paese dell'UE adotta linee guida comuni per riflettere:
- Diversità linguistica (ad esempio, Belgio, Spagna)
- Leggi nazionali e aspettative delle autorità sanitarie
- Considerazioni sull'accessibilità come Braille il contrasto cromatico
- Sicurezza del paziente grazie ad avvisi localizzati o miglioramenti digitali
Come Freyr Solutions supporta la conformità dell'Artwork UE
In Freyr Solutions, offriamo servizi specializzati di Artwork normativo per il mercato europeo, tra cui:
- Sviluppo di etichette multilingue per imballaggi esterni e interni
- Opere d'arte specifiche per paese da presentare e da commercializzare
- Integrazione Braille Blue Box
- Revisione normativa e controlli di qualità
- Gestione del ciclo di vita dell'Artwork per i prodotti nell'UE
Che si tratti del lancio di un prodotto in un singolo paese dell'UE o in tutta la regione, Freyr il vostro packaging sia pronto per la verifica, accurato e conforme agli standard sia dell'UE che locali. Inoltre, il design adattabile da un paese all'altro è molto fluido.