
Il Sistema informativo sulle sperimentazioni cliniche (CTIS) è una banca dati centralizzata che supporta lo svolgimento delle sperimentazioni cliniche nell'Unione europea (UE). È stato lanciato nel gennaio 2022 ed è una componente fondamentale del regolamento sulle sperimentazioni cliniche (CTR), che mira a migliorare l'efficienza e la trasparenza delle sperimentazioni cliniche nell'UE. Il CTIS una serie di caratteristiche che lo rendono uno strumento prezioso per gli sponsor delle sperimentazioni cliniche, i ricercatori e le autorità di regolamentazione.
Queste caratteristiche includono:
- Un unico punto di accesso per la presentazione e la gestione di studi clinici in più Paesi.
- Un modo sicuro ed efficiente per scambiare informazioni tra sponsor, ricercatori e autorità di regolamentazione.
- Un database ricercabile di studi clinici accessibile al pubblico.
- Strumenti a supporto del monitoraggio e della supervisione delle sperimentazioni cliniche.
- CTIS già avendo un impatto positivo sul panorama delle sperimentazioni cliniche nell'UE. Rende più facile e veloce condurre sperimentazioni cliniche e garantisce che i dati delle sperimentazioni cliniche siano più trasparenti e accessibili.
Scopri CTIS per le tue sperimentazioni cliniche
Ottimizzate ora i vostri studi clinici
Come CTIS cambiando il panorama delle sperimentazioni cliniche:
- Il CTIS sta facilitando la conduzione di sperimentazioni cliniche in più paesi:
In precedenza, gli sponsor dovevano presentare domande separate a ciascun paese in cui desideravano condurre una sperimentazione clinica. Si trattava di un processo lungo e costoso. CTIS agli sponsor di presentare un'unica domanda valida in tutti Member States dell'UE. Ciò ha reso molto più semplice e veloce per gli sponsor condurre sperimentazioni cliniche in più paesi.
- Il CTIS sta migliorando l'efficienza del processo di revisione delle sperimentazioni cliniche:
Le autorità di regolamentazione dei diversi paesi possono ora collaborare più facilmente attraverso CTIS. Ciò significa che le richieste possono ora essere esaminate in modo più rapido ed efficiente.
- CTIS rendendo più trasparenti i dati relativi alle sperimentazioni cliniche:
Il sito web pubblico del CTIS accesso alle informazioni relative a tutte le sperimentazioni cliniche registrate nel sistema. Tali informazioni includono il protocollo della sperimentazione, i risultati della sperimentazione ed eventuali problemi di sicurezza. Questa maggiore trasparenza contribuisce a rafforzare la fiducia del pubblico nelle sperimentazioni cliniche.
CTIS uno strumento prezioso che aiuta ad affrontare alcune delle sfide chiave che si presentano durante gli studi clinici. Rendendo più facile, veloce e trasparente la conduzione degli studi clinici, CTIS portare rapidamente nuovi trattamenti ai pazienti.
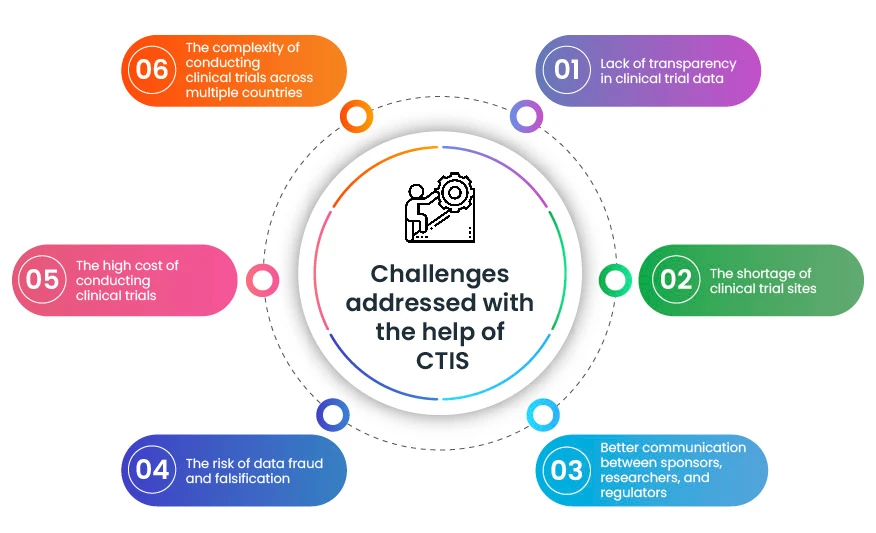
CTIS ancora un sistema relativamente nuovo, ma ha il potenziale per rivoluzionare il modo in cui vengono condotti gli studi clinici nell'UE. In un mondo in cui i progressi scientifici sono più importanti che mai, CTIS, in sinergia con un partner normativo globale come Freyr, detiene la chiave per aprire nuove frontiere nell'assistenza sanitaria. Abbracciando queste tecnologie trasformative, apriamo la strada a scoperte più rapide, sicure e di maggiore impatto, che hanno il potenziale di plasmare il futuro della medicina per le generazioni a venire.









