A livello globale, le Agenzie Sanitarie richiedono ai produttori stranieri di dispositivi medici e IVD di nominare un rappresentante locale. In Giappone, ai sensi della legge rivista sui prodotti farmaceutici e dispositivi medici (PMD), il sistema In-Country Caretaker (ICC) è stato sostituito dal sistema Marketing Authorization Holder (MAH). Secondo questo sistema, le aziende devono ottenere una licenza MAH per ottenere l'approvazione del dispositivo e commercializzare i dispositivi in Giappone.
Il titolare dell'autorizzazione all'immissione in commercio (MAH) deve essere un soggetto locale con sede in Giappone. produttori nazionali produttori ottenere direttamente la licenza MAH, mentre i produttori stranieri devono individuare un soggetto locale che soddisfi tale requisito MAH.
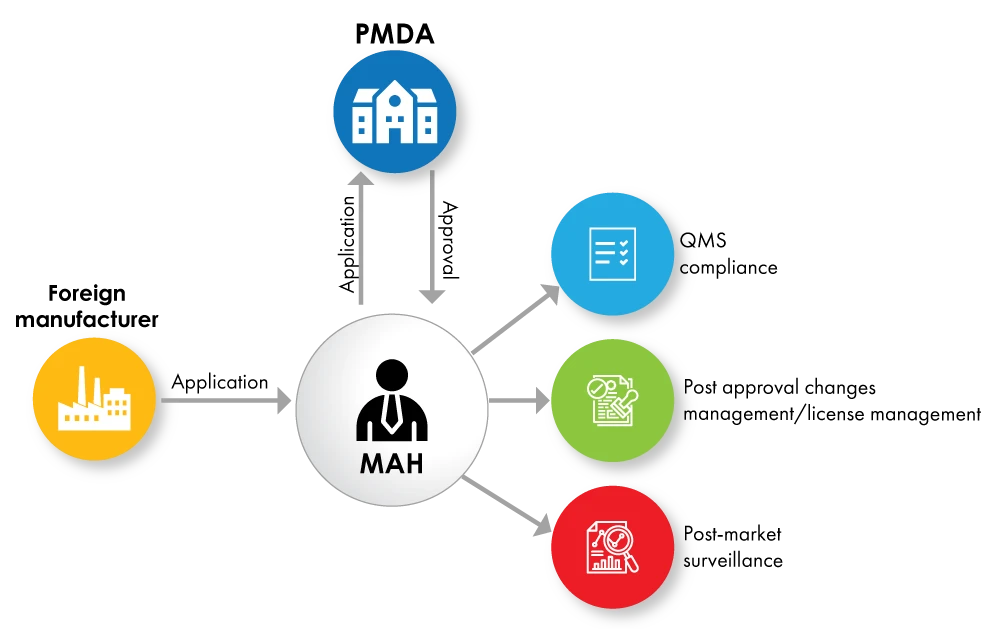
Fig. n. 1: Diagramma di flusso della registrazione del dispositivo con MAH come titolare di licenza
Se i produttori stranieri non desiderano cedere la piena proprietà del prodotto al MAH, possono nominare un Titolare dell'Autorizzazione all'Immissione in Commercio Designato (DMAH). Il DMAH presenta la domanda per conto del produttore straniero e l'approvazione viene concessa al produttore straniero per il dispositivo.
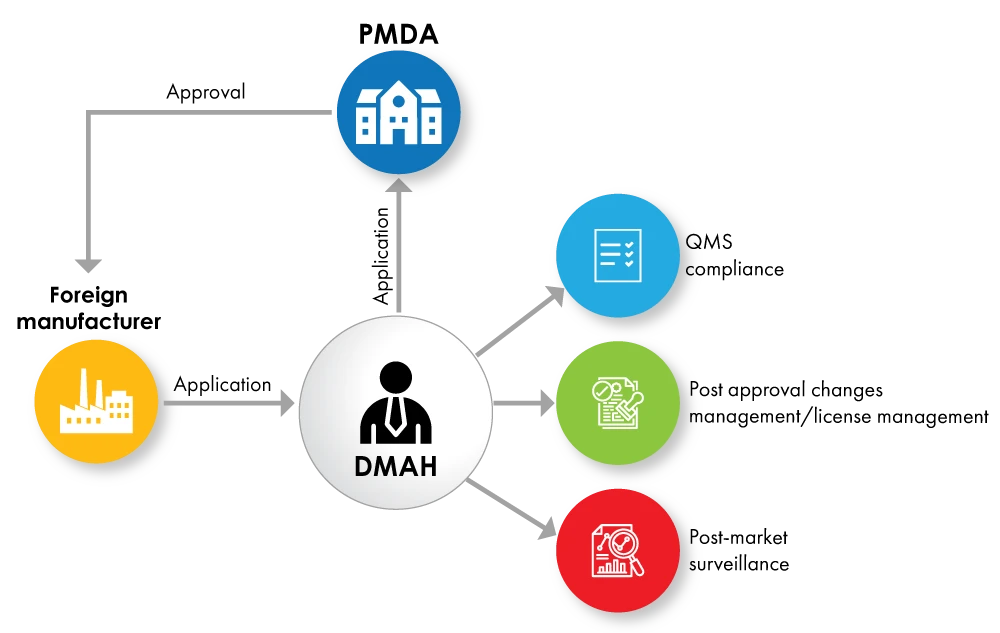
Fig. 2: Diagramma di flusso della registrazione del dispositivo con DMAH come titolare di licenza
Esistono tre (03) possibili opzioni attraverso le quali il produttore straniero può soddisfare i requisiti MAH PMDA. produttori stranieri produttori valutare attentamente tutte e tre (03) le possibilità. Esse includono:
Stabilire una filiale in Giappone
I produttori stranieri possono aprire un ufficio locale in Giappone e agire come Market Authorization Holder (MAH) per lanciare i loro prodotti in Giappone. Ciò consente al produttore straniero di avere la piena proprietà e una visibilità completa dei propri prodotti in Giappone. Questa potrebbe non essere una scelta preferita per i produttori di piccole dimensioni, poiché il costo associato all'apertura di una filiale in Giappone e al mantenimento dei requisiti di qualità del Ministero della Salute, del Lavoro e del Welfare (MHLW) è piuttosto elevato.
Distributore come MAH
È un modo conveniente per i produttori stranieri che non hanno un ufficio locale in Giappone. Gli importatori o i distributori possono essere nominati come MAH o DMAH. Considerando i ricavi generati dalle vendite dei dispositivi, gli importatori e i distributori di solito non addebitano costi aggiuntivi per agire come MAH o DMAH. I produttori, tuttavia, affrontano sfide nel raggiungere la penetrazione del mercato poiché il distributore che agisce come MAH potrebbe non essere disposto a rilasciare un No Objection Certificate (NoC) ad altri distributori. I distributori, a volte, non collaborano con il produttore straniero nel cambiare il MAH e nel trasferire la licenza del dispositivo al MAH/DMAH appena identificato.
Alleanza di terze parti
I produttori stranieri possono nominare un fornitore di servizi terzo indipendente come loro Market Authorization Holder (MAH)/DMAH. La riservatezza del dispositivo è ben protetta e il produttore straniero controlla la proprietà legale del prodotto. I produttori possono implementare e realizzare i loro piani di espansione del mercato.
Responsabilità del titolare dell'autorizzazione all'immissione in commercio
Un MAH/DMAH agisce come rappresentante per conto del produttore straniero e assiste nell'approvazione dei dispositivi in Giappone. Le principali responsabilità di un MAH/DMAH comprendono:
- End-to-end approvazione dei dispositivi.
- Garantire che i dispositivi sicuri e di qualità entrino nel mercato giapponese gestendo correttamente la produzione e il controllo di qualità dei prodotti.
- Essere responsabili dell'immissione del dispositivo alla parte che detiene una licenza di vendita/distribuzione di dispositivi medici.
- Gestione delle attività di Post-Market Surveillance (PMS)
Poiché il MAH/DMAH deve seguire tutte le misure di sicurezza, Quality Management System (QMS) e le Buone Pratiche di Vigilanza (GVP) per conto del produttore straniero, è estremamente importante scegliere il MAH/DMAH giusto. Pertanto, i produttori stranieri produttori valutare attentamente tutte le opzioni prima di optare per il miglior modello MAH possibile. Ciò include l'esecuzione di un'analisi di fattibilità, la determinazione del RoI, il rapporto con gli importatori e i distributori, il budget disponibile, la dimensione del portafoglio, il profitto per la vendita dei dispositivi, le tempistiche per il lancio dei dispositivi, ecc. produttori scegliere meticolosamente se assegnare la proprietà del dispositivo al MAH o nominare un DMAH e mantenere la proprietà con loro.
Per ulteriori informazioni sui requisiti MAH/DMAH in Giappone, reach un esperto in materia di regolamentazione di Freyr. Rimani informato. Rimani conforme.