
I dispositivi medici svolgono un ruolo vitale nel migliorare la salute dei pazienti, ma possono verificarsi non conformità nei dispositivi anche con i migliori sistemi di controllo qualità in atto. Le non conformità si riferiscono a casi in cui un prodotto o un processo non soddisfa i requisiti normativi, gli standard di qualità o le procedure interne approvate. Una gestione efficace delle non conformità è importante per garantire la sicurezza dei pazienti, la conformità normativa e la reputazione dei produttori di dispositivi medici.
Questo blog esplora l'importanza della gestione delle non conformità nei dispositivi medici, il processo e le migliori pratiche.
L'importanza della gestione delle non conformità nei dispositivi medici
Una gestione efficace delle non conformità può aiutare a identificare potenziali problemi precocemente, prevenire danni ai pazienti e migliorare la qualità complessiva dei dispositivi medici. Può anche aiutare i produttori a rispettare i requisiti normativi, mantenere la soddisfazione del cliente e, in definitiva, migliorare i risultati economici riducendo i costi e la manodopera associati a guasti e richiami di prodotti.
D'altra parte, se le non conformità non vengono identificate e affrontate tempestivamente, possono portare a un guasto del dispositivo, a una non conformità normativa e possono avere effetti dannosi sulla salute del paziente. Se un prodotto non conforme viene immesso sul mercato, può comportare costosi richiami, ripercussioni legali e danni alla reputazione del produttore.
Il processo di gestione delle non conformità nei dispositivi medici
Il processo di gestione delle non conformità nei dispositivi medici prevede diverse fasi, tra cui l'identificazione, l'indagine, l'analisi della causa principale (RCA), la valutazione dell'impatto e la pianificazione di azioni correttive e preventive (CAPA). Il processo deve essere ben documentato con rapporti sulle non conformità e tutte le parti interessate devono essere formate al processo per garantirne l'efficacia.
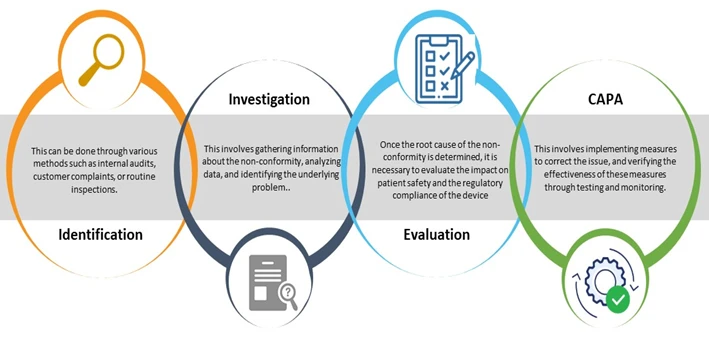
Cinque (05) pratiche da adottare per una gestione efficace delle non conformità nei dispositivi medici
Un'efficace gestione delle non conformità nei dispositivi medici richiede un approccio sistematico e proattivo per identificare e affrontare le non conformità. Di seguito sono riportate alcune delle migliori pratiche per un'efficace gestione delle non conformità nei dispositivi medici:
- Un solido Quality Management System (QMS)-: Stabilire e mantenere un QMS efficace che includa procedure per l'identificazione e la gestione delle non conformità.
Formazione del personale: Assicurarsi che tutto il personale sia formato sulle procedure di gestione delle non conformità, compreso il processo di identificazione, indagine, valutazione, valutazione dell'impatto e CAPA.
- Manutenzione dei registri: Mantenere tutti i registri e documentare tutte le informazioni relative al monitoraggio delle non conformità, alla RCA, alla valutazione dell'impatto e alla CAPA.
- Audit interni regolari: Condurre regolarmente audit interni per valutare l'efficacia del processo di gestione delle non conformità e identificare le aree di miglioramento.
Miglioramento continuo: Promuovere una cultura del miglioramento continuo incoraggiando il feedback di tutte le parti interessate, compresi clienti, fornitori e dipendenti.
È fondamentale implementare una gestione efficace delle non conformità per garantire la sicurezza del paziente, la conformità normativa e proteggere la reputazione dei produttori di dispositivi medici. È possibile raggiungere questo obiettivo creando un QMS robusto in grado di identificare e affrontare accuratamente le non conformità, prevenendone in ultima analisi l'occorrenza e migliorando la qualità complessiva dei dispositivi medici. Create un QMS robusto per il vostro dispositivo medico e assicuratene la conformità e la sicurezza del paziente con l'assistenza dei nostri esperti normativi. Rimanete informati! Rimanete conformi!









