Artwork w zakresie zgodnych z przepisami farmaceutycznymi Artwork
Zapewnienie zgodnych z przepisami i efektownych artwork opakowań farmaceutycznych artwork pomysłu do wprowadzenia na rynek.
Przeglądaj tematy
- Czym są Artwork regulacyjnej?
- Jakie są kluczowe elementy artwork związanych z artwork regulacyjną?
- Jakie znaczenie ma zgodność z przepisami w przemyśle farmaceutycznym?
- Przegląd wymogów regulacyjnych dotyczących Artwork branży farmaceutycznej
- Jaki wpływ mają postępy technologiczne na regulacje Artwork?
- Globalne organy regulacyjne i wytyczne
- Jakie są kluczowe przepisy i normy dotyczące Artwork farmaceutycznej?
- Jaki jest wpływ nieprzestrzegania przepisów dotyczących Artwork regulacyjnej?
- Jakie wyzwania związane z Artwork napotykają firmy farmaceutyczne?
- W jaki sposób Twój zespół zajmuje się Artwork ?
- Jakie są oznaki, że Twoja firma potrzebuje dostawcy Artwork ?
- Jakie są korzyści ze współpracy z dostawcą Artwork ?
- Jak Freyr może ci pomóc na całym świecie?
- Dlaczego Freyr?
- Nasze usługi
Czym są Artwork regulacyjnej?
Ostatnia aktualizacja na: Wrzesień, 2024
W ściśle regulowanej branży farmaceutycznej artwork odgrywają kluczową rolę w zapewnieniu tworzenia, zarządzania i przedkładania artwork z rygorystycznymi normami regulacyjnymi. Usługi te obejmują specjalistyczny zakres rozwiązań mających na celu zagwarantowanie zgodności z globalnymi przepisami i normami dotyczącymi etykiet, opakowań i innych materiałów drukowanych związanych z produktami farmaceutycznymi. Dzięki wiedzy specjalistycznej w zakresie artwork , zgodności etykiet, lokalizacji, tłumaczeń, informacji regulacyjnych, zarządzaniaartwork i zapewnienia jakości, artwork regulacyjnej są niezbędne dla firm farmaceutycznych, które chcą sprawnie poruszać się w złożonym środowisku regulacyjnym. Ich skrupulatna dbałość o szczegóły zapewnia bezpieczeństwo pacjentów, promuje zgodność z przepisami i ułatwia płynne wprowadzanie produktów farmaceutycznych na rynek.
Ponadto, w środowisku, w którym wymagania regulacyjne nieustannie ewoluują, artwork regulacyjnej zapewniają firmom farmaceutycznym stałe wsparcie i doradztwo. Dzięki śledzeniu na bieżąco aktualizacji przepisów i stosowaniu najlepszych praktyk usługi te gwarantują zgodność opakowań i etykiet produktów farmaceutycznych z najnowszymi regulacjami, ograniczając tym samym ryzyko i zapewniając integralność produktu przez cały cykl jego życia.

Jakie są kluczowe elementy artwork związanych z artwork regulacyjną?
Kluczowe elementy artwork związanych z artwork regulacyjną wspólnie przyczyniają się do zapewnienia zgodności z wymogami regulacyjnymi, poprawy jakości i skuteczności opakowań i etykiet produktów farmaceutycznych oraz ochrony zdrowia i bezpieczeństwa pacjentów.
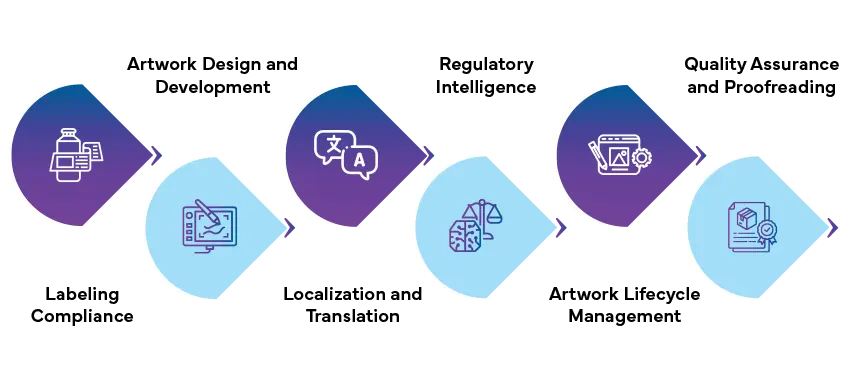
Zgodność z etykietami
- Dbanie o to, by etykiety produktów zawierały dokładne i zgodne z przepisami informacje.
- Przeglądanie i weryfikacja treści etykiet pod kątem dokładności, kompletności i zgodności z wytycznymi regulacyjnymi.
- Wytyczne dotyczące projektu etykiety, formatu, rozmiarów czcionek i symboli w celu zapewnienia zgodności i czytelności.
Artwork i opracowywanie Artwork
- Współpraca z grafikami i ekspertami ds. regulacji w celu tworzenia artwork spełniają wymogi regulacyjne, zachowując jednocześnie tożsamość marki.
- Opracowywanie projektów opakowań, które skutecznie przekazują istotne informacje użytkownikom końcowym, w tym instrukcje dotyczące dawkowania, ostrzeżenia i środki ostrożności.
- Uwzględnienie symboli regulacyjnych, ikon i ostrzeżeń zgodnie z wytycznymi regulacyjnymi.
Lokalizacja i tłumaczenie
- Dostosowywanie artwork etykiet do różnych rynków i języków, aby spełniały regionalne wymogi regulacyjne.
- Dokładne tłumaczenie treści etykiet przy jednoczesnym zapewnieniu adekwatności językowej i kulturowej.
- Przeprowadzanie walidacji językowej i kontroli jakości w celu weryfikacji dokładności i spójności tłumaczonych treści.
Wywiad regulacyjny
- Monitorowanie zmian i aktualizacji przepisów, które mogą mieć wpływ na artwork .
- Dostarczanie aktualnych informacji i wskazówek na temat zmieniających się standardów i wytycznych regulacyjnych.
- Pomoc firmom farmaceutycznym w poruszaniu się po złożonym środowisku regulacyjnym i dostosowywaniu artwork zmian regulacyjnych.
Zarządzanie Artwork
- Zarządzanie całym artwork , od opracowania koncepcji po ostateczne zatwierdzenie i produkcję.
- Wdrożenie procesów kontroli zmian w celu śledzenia i zarządzania artwork oraz aktualizacjami artwork .
- Zapewnienie spójności, dokładności i zgodności między artwork i iteracjami artwork .
Zapewnienie jakości i korekta
- Przeprowadzanie przeglądów zapewnienia jakości i kontroli korekty w celu identyfikacji błędów, niespójności i odchyleń od wymogów regulacyjnych.
- Wdrażanie rygorystycznych procesów kontroli jakości w celu zapewnienia, że artwork najwyższe standardy jakości i dokładności.
- Przedstawianie zaleceń i działań naprawczych w celu rozwiązania zidentyfikowanych problemów i poprawy artwork .
Jakie znaczenie ma zgodność z przepisami w przemyśle farmaceutycznym?
Zgodność z przepisami w sektorze farmaceutycznym odnosi się do przestrzegania określonych przepisów i statutów ustanowionych przez organy regulacyjne rządzące branżą. Wymóg ten obejmuje kompleksowe zrozumienie odpowiednich przepisów i regulacji mających zastosowanie do działalności biznesowej, a następnie skrupulatne przestrzeganie tych mandatów w celu złagodzenia potencjalnych kar lub reperkusji prawnych. W branży farmaceutycznej zgodność z przepisami obejmuje różne aspekty, od zapewnienia bezpieczeństwa produktów po utrzymanie etycznych praktyk marketingowych.
Znaczenie zgodności z przepisami jest nie do przecenienia, ponieważ służy ona jako zabezpieczenie, chroniąc konsumentów przed potencjalnymi zagrożeniami związanymi z produktami lub usługami, jednocześnie zapewniając zgodne z prawem postępowanie przedsiębiorstw. Nieprzestrzeganie przepisów pociąga za sobą poważne konsekwencje, w tym wysokie grzywny, a w poważnych przypadkach zarzuty karne. W związku z tym przedsiębiorstwa farmaceutyczne muszą pilnie przestrzegać standardów zgodności, aby zapobiegać takim niekorzystnym skutkom.
Utrzymanie ciągłej zgodności wymaga proaktywnego podejścia, pociągającego za sobą ciągłą czujność w zakresie rozwoju branży i aktualizacji przepisów. Wiąże się to z częstym monitorowaniem autorytatywnych platform rządowych pod kątem zmian legislacyjnych i subskrybowaniem odpowiednich publikacji w celu uzyskania wglądu w zmiany regulacyjne. Ponadto dogłębne zrozumienie obowiązków organizacyjnych wynikających z obowiązujących przepisów jest niezbędne do sformułowania i realizacji kompleksowej strategii zgodności, zapewniając w ten sposób trwałe przestrzeganie mandatów regulacyjnych.
Przegląd wymogów regulacyjnych dotyczących Artwork branży farmaceutycznej
W sektorze farmaceutycznym przestrzeganie przepisów regulacyjnych dotyczących artwork zasadnicze artwork dla zapewnienia skutecznego i bezpiecznego stosowania Produkty lecznicze jednoczesnym spełnieniu wymogów prawnych. Wymogi te obejmują szeroki zakres dyrektyw i norm regulujących koncepcję, treść i prezentację opakowań i etykiet produktów farmaceutycznych.
Przede wszystkim artwork farmaceutyczna artwork być zgodna z przepisami określonymi przez autorytatywne agencje zdrowia, takie jak Agencja ds. Żywności i Leków (FDA w Stanach Zjednoczonych, Europejska Agencja Leków (EMA) w Europie oraz analogiczne podmioty na całym świecie. Przepisy te nakładają obowiązek umieszczania na opakowaniach i etykietach kluczowych informacji, obejmujących identyfikację produktu, instrukcje dotyczące dawkowania, ostrzeżenia, przeciwwskazania i daty ważności.
Co więcej, przestrzeganie określonych protokołów formatowania i projektowania jest niezbędne do zapewnienia spójności, czytelności i jednolitości w różnych formatach i wymiarach opakowań. Wymaga to przestrzegania kryteriów dotyczących wymiarów czcionek, zróżnicowania kolorów i strategicznego rozmieszczenia istotnych szczegółów w celu zoptymalizowania przejrzystości i zmniejszenia prawdopodobieństwa błędów medycznych.
Ponadto artwork zatwierdzeniem do wdrożenia artwork dotyczących produktów farmaceutycznych konieczne jest podjęcie rygorystycznych środków zapewnienia jakości w celu potwierdzenia ich dokładności, kompletności i zgodności z przepisami. Zazwyczaj wymaga to przeprowadzenia kompleksowych ocen przez Sprawy regulacyjne , specjalistów ds. zapewnienia jakości, a czasami również zewnętrznych doradców ds. regulacyjnych w celu wykrycia i skorygowania wszelkich odchyleń lub niezgodności.
Podsumowując, zgodność z dyrektywami regulacyjnymi dotyczącymi artwork farmaceutycznej artwork niezbędna dla zapewnienia dobrobytu pacjentów, zachowania skuteczności produktów oraz ograniczenia zagrożeń prawnych i regulacyjnych związanych z nieprzestrzeganiem przepisów. Przedsiębiorstwa farmaceutyczne muszą zachować czujność w monitorowaniu zmieniających się ram regulacyjnych i stale udoskonalać swoje artwork , aby zapewnić zgodność z przepisami i utrzymać niezrównane standardy jakości i bezpieczeństwa swoich produktów.
Jaki wpływ mają postępy technologiczne na regulacje Artwork?
artwork regulacyjnej przeszedł znaczącą transformację w wyniku ciągłego postępu technologicznego. Postępy te nie tylko usprawniły działalność, ale także podniosły precyzję, skuteczność i zgodność z normami regulacyjnymi w dziedzinie farmaceutycznej.
Oto dogłębna analiza wpływu technologii na artwork regulacyjne:
Zwiększona wydajność operacyjna i optymalizacja procesów
- Wykorzystanie oprogramowania Artwork i zarządzania Artwork : Specjalistyczne narzędzia programowe zastąpiły metody ręczne, ułatwiając efektywne opracowywanie, modyfikowanie i kontrolowanie wersji artwork.
- Przejście na zgłoszenia elektroniczne: Powszechne przyjęcie przez agencje regulacyjne elektronicznych systemów składania wniosków wyeliminowało zależność od dokumentacji papierowej, co w konsekwencji przyspieszyło procesy zatwierdzania.
- Integracja platform współpracy: Platformy internetowe służą jako kanały płynnej współpracy między zainteresowanymi stronami, wspierając lepszą komunikację i usprawniając procedury przeglądu i zatwierdzania.
Zwiększona precyzja i integralność danych
- Zautomatyzowane mechanizmy wprowadzania danych: Integracja z systemami korporacyjnymi, takimi jak Product Information Management (PIM), ogranicza błędy związane z ręcznym wprowadzaniem danych, zapewniając jednolitość artwork .
- Wdrożenie podpisów cyfrowych i ścieżek audytu: Funkcje podpisu elektronicznego i kompleksowe ścieżki audytu wzmacniają integralność danych i identyfikowalność w całym artwork .
- Wykorzystanie narzędzi walidacyjnych: Zautomatyzowane narzędzia walidacyjne identyfikują potencjalne rozbieżności w artwork , ograniczając ryzyko niezgodności.
Zwiększona dostępność do rynków globalnych i inicjatywy harmonizacyjne
- Wdrożenie systemów zarządzania tłumaczeniami: Rozwiązania programowe przyspieszają tłumaczenie i lokalizację artwork różnych rynków globalnych, zapewniając zgodność z przepisami i dostosowanie do zróżnicowanej demografii pacjentów.
- Dostęp do baz danych informacji regulacyjnych: Repozytoria online zapewniają dostęp do przepisów i wytycznych z wielu jurysdykcji, ułatwiając zachowanie zgodności z przepisami w skali globalnej.
- Promowanie inicjatyw harmonizacyjnych: Współpraca między organami regulacyjnymi sprzyja ujednoliceniu wymagań dotyczących etykietowania, upraszczając artwork na rynki międzynarodowe.
Eksploracja nowych technologii
- Integracja sztucznej inteligencji (AI): Rozwiązania oparte na sztucznej inteligencji analizują artwork niezgodności, automatyzują powtarzalne zadania i personalizują informacje o pacjentach w celu zwiększenia zaangażowania.
- Wdrożenie rzeczywistości rozszerzonej (AR): Technologia AR nakłada interaktywne informacje na opakowania, zapewniając pacjentom dodatkowe informacje o produkcie i instrukcje użytkowania.
- Wykorzystanie technologii blockchain: Technologia blockchain zwiększa bezpieczeństwo danych i identyfikowalność w całym artwork , promując zaufanie i przejrzystość w ramach regulacyjnych.
Postęp technologiczny wywarł głęboki wpływ artwork regulacyjną, torując drogę do bardziej wydajnego, dokładnego i globalnie dostępnego środowiska. Wykorzystanie tych innowacji i proaktywne podejście do związanych z nimi wyzwań pozwala firmom zachować zgodność z przepisami, skuteczność i zdolność reagowania na zmieniające się wymagania pacjentów i organów regulacyjnych w dynamicznym sektorze farmaceutycznym.
Globalne organy regulacyjne i wytyczne
Poruszanie się po skomplikowanym świecie globalnych przepisów dotyczących artwork farmaceutycznej artwork ogromne wyzwanie. W tej sekcji omówiono najważniejsze organy regulacyjne i odpowiadające im wytyczne, aby dostarczyć Państwu niezbędnych informacji:
Poruszanie się po skomplikowanym świecie globalnych przepisów dotyczących artwork farmaceutycznej artwork ogromne wyzwanie. W tej sekcji omówiono najważniejsze organy regulacyjne i odpowiadające im wytyczne, aby dostarczyć Państwu niezbędnych informacji:
Amerykańska Agencja ds. Żywności i LekówFDA)
Władze: FDA nadzoruje etykietowanie i pakowanie leków dla ludzi i leków weterynaryjnych w Stanach Zjednoczonych.
Kluczowe wytyczne:
- Kodeks przepisów federalnych (CFR), tytuł 21, części 201 i 601: Sekcje te określają wymagania dotyczące etykietowania leków i produktów biologicznych.
- Wytyczne dla przemysłu: Etykietowanie leków wydawanych na receptę i bez recepty: Dokument ten zawiera kompleksowe zalecenia dotyczące treści, formatu i prezentacji etykiet.
- Wytyczne Międzynarodowej Rady Harmonizacji Wymagań Technicznych dla Środków Farmaceutycznych Stosowanych u LudziICH): FDA często przyjmuje i odwołuje się do odpowiednich wytycznych ICH dotyczących standardów etykietowania.
Europejska Agencja LekówEMA)
Uprawnienia: EMA jurysdykcję w zakresie wydawania zezwoleń i nadzoru nad Produkty lecznicze stosowania u ludzi i zwierząt w całej Unii Europejskiej (UE).
Kluczowe wytyczne:
- Rozporządzenie Komisji (WE) nr 726/2004: Rozporządzenie to określa wymagania dotyczące etykietowania Produkty lecznicze ludzi w UE.
- Wytyczne dotyczące Labelling Produkty lecznicze ludzi: Niniejsza dyrektywa zawiera wyczerpujące wytyczne dotyczące treści, formatu i prezentacji etykiet.
- Wytyczne ICH : Analogicznie do FDA, EMA uwzględnia i odnosi się do odpowiednich wytycznych ICH dotyczących protokołów etykietowania.
Światowa Organizacja ZdrowiaWHO)
Władze: WHO zapewnia globalne przywództwo i wytyczne w zakresie przepisów farmaceutycznych, dążąc do harmonizacji i standaryzacji na całym świecie.
Kluczowe wytyczne:
- Załącznik 9 do wytycznych WHO dotyczących dobrych praktyk wytwarzania (GMP): Załącznik ten zawiera zalecenia dotyczące etykietowania i pakowania produktów farmaceutycznych.
- Wzorcowe listy podstawowych leków WHO : Listy te zalecają stosowanie podstawowych leków w różnych placówkach opieki zdrowotnej, często wraz z określonymi przepisami dotyczącymi etykietowania.
Międzynarodowa Rada HarmonizacjiICH)
Rola: ICH stanowi globalną inicjatywę obejmującą organy regulacyjne z Europy, Japonii, Stanów Zjednoczonych i innych regionów.
Wytyczne: ICH formułuje zharmonizowane wytyczne dotyczące różnych aspektów rozwoju farmaceutycznego, w tym protokołów etykietowania.
ICH Q3C: Niniejsze wytyczne zawierają zalecenia dotyczące opracowywania i uzasadniania etykiet oraz ulotek dołączanych do opakowań Produkty lecznicze stosowanych u ludzi.
Inne regionalne organy regulacyjne
Kilka regionalnych organów regulacyjnych ogłasza swoje szczegółowe wytyczne dotyczące artwork farmaceutycznej, często dostosowując się do zasad ustanowionych przez władze lub odwołując się do nich. Godne uwagi przykłady obejmują:
- Chińska Krajowa Administracja Produktów MedycznychNMPA)
- Japońska wyroby medyczne ds. Produktów Leczniczych i wyroby medyczne (PMDA)
- Health Canada
Jakie są kluczowe przepisy i normy dotyczące Artwork farmaceutycznej?
Istnieją ważne przepisy i normy regulujące artwork z artwork farmaceutyczną, artwork zapewnienie zgodności z wymogami regulacyjnymi i promowanie bezpieczeństwa pacjentów. Oto najważniejsze przepisy i normy dotyczące artwork farmaceutycznej:
Przepisy FDA dotyczące etykietowania (Stany Zjednoczone)
- Kodeks przepisów federalnych (CFR), tytuł 21, części 201 i 314: Określa wymogi dotyczące etykietowania leków na receptę i bez recepty, w tym specyfikacje dotyczące treści, formatu i umieszczania informacji na etykietach i opakowaniach.
Przepisy EMA dotyczące etykietowania (Unia Europejska)
- Rozporządzenie Komisji (WE) nr 726/2004: Określa wymagania dotyczące etykietowania Produkty lecznicze ludzi w UE, obejmujące takie aspekty, jak treść, forma prezentacji i wymagania językowe.
- Wytyczne dotyczące Labelling Produkty lecznicze ludzi: Zawiera szczegółowe wytyczne dotyczące treści i formatu etykiet, w tym wymagania dotyczące czytelności i zrozumiałości.
Wytyczne ICH
- ICH (Jakość produktów biotechnologicznych: Badania stabilności produktów biotechnologicznych/biologicznych): Wytyczne dotyczące projektu i treści ulotek dołączanych do produktów biotechnologicznych, w tym uwagi dotyczące artwork.
- ICH (R2) Rozwój farmaceutyczny: Oferuje zasady rozwoju farmaceutycznego, w tym uwagi dotyczące etykietowania i artwork cyklu życia produktu.
Normy ISO
- ISO 11607 (Opakowania dla wyroby medyczne poddanych sterylizacji końcowej): Określa wymagania dotyczące projektowania, walidacji i etykietowania opakowań dla wyroby medyczne poddanych sterylizacji końcowej, zapewniając bezpieczeństwo i skuteczność.
- ISO 13485 wyroby medyczne systemy zarządzania jakością): Określa wymagania dotyczące systemów zarządzania jakością w projektowaniu i produkcji wyroby medyczne, w tym kwestie związane z etykietowaniem.
Normy Farmakopealne
- Farmakopea Stanów Zjednoczonych (USP): Zapewnia standardy etykietowania, pakowania i przechowywania produktów farmaceutycznych, zapewniając ich jakość i bezpieczeństwo.
- Farmakopea Europejska (Ph. Eur.): Zawiera monografie i wytyczne dotyczące etykietowania farmaceutycznego i materiałów opakowaniowych, zapewniając zgodność z wymogami prawnymi w Europie.
Wytyczne dotyczące dobrej praktyki produkcyjnej (GMP)
- PrzepisyFDA GMP (21 CFR część 210 i 211): Określają wymagania dotyczące produkcji, etykietowania i pakowania produktów farmaceutycznych w celu zapewnienia jakości i bezpieczeństwa.
- Wytyczne GMP UE: Nakreślenie zasad i wytycznych dotyczących produkcji farmaceutycznej, w tym wymogów dotyczących etykietowania i pakowania w celu zapewnienia jakości produktu i bezpieczeństwa pacjentów.
Krajowe przepisy i wytyczne
- PrzepisyHealth Canada : Regulują wymagania dotyczące etykietowania produktów farmaceutycznych w Kanadzie, zapewniając zgodność ze standardami bezpieczeństwa i skuteczności.
- Przepisy Japońskiej wyroby medyczne ds. Produktów Leczniczych i wyroby medyczne (PMDA): Określają wymagania dotyczące etykietowania i pakowania produktów farmaceutycznych w Japonii, zapewniając jakość i bezpieczeństwo produktów.
Przestrzeganie tych przepisów i norm ma zasadnicze znaczenie dla firm farmaceutycznych w celu zapewnienia zgodności, promowania bezpieczeństwa pacjentów i ułatwienia dostępu do rynku dla ich produktów. Zgodność z tymi wymogami pomaga ograniczać ryzyko i zapewnia jakość, skuteczność i bezpieczeństwo produktów farmaceutycznych.
Jaki jest wpływ nieprzestrzegania przepisów dotyczących Artwork regulacyjnej Artwork
Nieprzestrzeganie artwork regulacyjnych artwork ma poważne konsekwencje dla firm farmaceutycznych, zarówno w zakresie zdrowia publicznego, jak i działalności biznesowej. Niezgodność z artwork regulacyjnymi artwork wielowymiarowe ryzyko dla przedsiębiorstw farmaceutycznych, obejmujące aspekty prawne, finansowe, reputacyjne i operacyjne. Proaktywne przestrzeganie protokołów zgodności, solidne ramy zapewnienia jakości i ciągła czujność regulacyjna są niezbędne do ograniczenia tego ryzyka i utrzymania integralności regulacyjnej w artwork farmaceutycznej.
Poniżej znajduje się dogłębna analiza konsekwencji wynikających z nieprzestrzegania przepisów:
Obawy dotyczące bezpieczeństwa pacjentów
- Odstępstwa od norm regulacyjnych w artwork skutkować nieścisłościami lub pominięciami w informacjach farmaceutycznych, zwiększając ryzyko błędów w stosowaniu leków lub działań niepożądanych u pacjentów.
- Nieodpowiednie oznakowanie lub opakowanie może powodować nieporozumienia dotyczące wytycznych dawkowania, przeciwwskazań lub instrukcji przechowywania, zagrażając tym samym dobru pacjenta.
Kary regulaminowe i grzywny
- Organy regulacyjne nakładają surowe kary za nieprzestrzeganie artwork dotyczących artwork , obejmujące kary pieniężne, wycofanie produktów z rynku oraz środki egzekucyjne.
- Niespełnienie kryteriów regulacyjnych może utrudnić uzyskanie zezwoleń rynkowych, opóźniając wprowadzenie produktu na rynek i strategie wejścia na rynek.
Uszkodzenie reputacji
- Niezgodność podważa reputację i wiarygodność podmiotów farmaceutycznych, zmniejszając zaufanie wśród pracowników służby zdrowia, pacjentów i agencji regulacyjnych.
- Negatywny rozgłos wynikający z naruszeń przepisów lub wycofywania produktów z rynku może mieć długotrwały negatywny wpływ na postrzeganie marki i jej pozycję na rynku.
Odpowiedzialność prawna i spory sądowe
- Nieprawidłowe artwork firmy na ryzyko prawne, w tym potencjalne pozwy i spory sądowe ze strony poszkodowanych stron lub organów regulacyjnych.
- Finansowe koszty sporów sądowych, ugód i odszkodowań mogą powodować znaczne komplikacje i zakłócać ciągłość operacyjną.
Zakłócenia w łańcuchu dostaw
- Naruszenia przepisów dotyczących artwork spowodować wycofanie produktów z rynku lub nałożenie sankcji, zakłócając łańcuchy dostaw i powodując straty magazynowe, opóźnienia w produkcji oraz komplikacje logistyczne.
- Takie zakłócenia osłabiają strumienie przychodów, relacje z klientami i ogólną odporność biznesową.
Utrata dostępu do rynku
- Niezgodność może spowodować ograniczenia rynkowe, wycofanie produktów lub utratę pozycji rynkowej w dotkniętych jurysdykcjach, ograniczając perspektywy przychodów i udział w rynku.
- Odbudowa zaufania organów regulacyjnych i przywrócenie obecności na rynku po incydentach niezgodności wymaga znacznego czasu, zasobów i strategicznych przedsięwzięć.
Zwiększona kontrola regulacyjna
- Niezgodność z przepisami prowadzi do wzmożonej kontroli, powodując intensyfikację audytów, inspekcji i nadzoru zgodności z przepisami ze strony organów regulacyjnych.
- Wzmożony nadzór regulacyjny pociąga za sobą dodatkowe obciążenia administracyjne, wydatki związane z przestrzeganiem przepisów i alokację zasobów na działania naprawcze.
Wada konkurencyjna
- Niezgodność z przepisami obniża konkurencyjność, ponieważ zgodne z przepisami odpowiedniki zyskują przewagę rynkową, wiarygodność i przychylność konsumentów.
- Niespełnienie kryteriów regulacyjnych może zniechęcić potencjalnych partnerów, inwestycje lub patronat, ograniczając perspektywy ekspansji biznesowej.
Jakie wyzwania związane z Artwork napotykają firmy farmaceutyczne?
Poruszanie się artwork zawiłościach artwork farmaceutycznej artwork ściśle regulowanym środowisku stanowi szczególne wyzwanie dla firm działających w tej branży. Osiągnięcie delikatnej równowagi między kreatywnością, precyzją i przestrzeganiem norm regulacyjnych wymaga skrupulatnego planowania i proaktywnego podejścia. Poniżej przedstawiono kilka głównych przeszkód napotykanych przez firmy farmaceutyczne w zarządzaniu artwork:
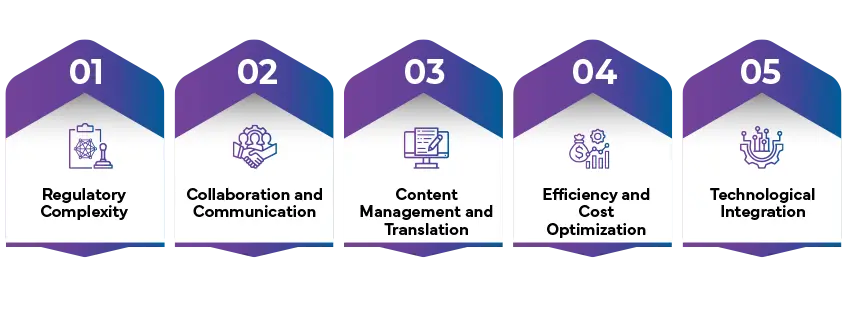
Złożoność przepisów
- Ciągłe zmiany regulacyjne: Nadążanie za nieustannie zmieniającymi się przepisami w różnych regionach stanowi ogromne wyzwanie. Artwork być zgodna z określonymi kryteriami dotyczącymi treści, formatu, języka i symboliki, które różnią się w zależności od rynku docelowego.
- Interpretacja wytycznych: Dokładne rozszyfrowanie i wdrożenie dyrektyw regulacyjnych wymaga specjalistycznej wiedzy i skrupulatnej dbałości o szczegóły, aby uniknąć pułapek niezgodności.
Współpraca i komunikacja
- Wielowymiarowi interesariusze: Proces artwork angażuje szerokie spektrum interesariuszy, w tym projektantów, zespoły marketingowe, ekspertów ds. regulacji i zewnętrznych współpracowników. Skuteczna koordynacja i komunikacja między tymi różnorodnymi podmiotami ma zasadnicze znaczenie dla zapewnienia płynnego przebiegu pracy.
- Kontrola wersji i monitorowanie: Zarządzanie wieloma iteracjami artwork etapach przeglądu i zatwierdzania stanowi wyzwanie, wymagające solidnych mechanizmów śledzenia modyfikacji, zapobiegania błędom i utrzymania przejrzystości.
Zarządzanie treścią i tłumaczenie
- Precyzja i kompleksowość: Zapewnienie dokładności, kompletności i spójności wszystkich artwork , w tym instrukcji dotyczących dawkowania, ostrzeżeń i przeciwwskazań, ma kluczowe znaczenie dla ochrony dobra pacjentów.
- Względy kulturowe: Tłumaczenie treści na rynki globalne wymaga wrażliwości na niuanse kulturowe i niuanse regulacyjne, aby uniknąć błędnych interpretacji i ułatwić jasną komunikację.
Wydajność i optymalizacja kosztów
- Czasochłonne procedury: Skrupulatna kontrola i protokoły zatwierdzania wymagane przez przepisy mogą pochłaniać znaczną ilość czasu, potencjalnie utrudniając wprowadzanie produktów na rynek i wpływając na harmonogram dostępu do rynku.
- Alokacja zasobów: Skuteczne zarządzanie artwork i weryfikacją artwork oraz zapewnienie zgodności z przepisami wymaga dedykowanych zasobów i specjalistycznych kompetencji, co wiąże się z konsekwencjami finansowymi dla organizacji.
Integracja technologiczna
- Zgodność ze starszymi systemami: Integracja nowych technologii z istniejącymi systemami stanowi wyzwanie, potencjalnie ograniczając wydajność procesów i interoperacyjność danych.
- Bezpieczeństwo danych i zgodność z przepisami: Wdrożenie solidnych środków bezpieczeństwa danych jest niezbędne do ochrony wrażliwych danych pacjentów w całym artwork i przestrzegania rygorystycznych przepisów dotyczących prywatności danych.
W jaki sposób Twój zespół zajmuje się Artwork ?
Proces artwork jest złożonym procesem, który może trwać od kilku dni do kilku miesięcy. artwork i przygotowanie do produkcji nawet jednej artwork może wymagać zaangażowania zespołu projektowego, działu prawnego i wszystkich innych osób.
Aby uniknąć wyzwań związanych z gromadzeniem informacji zwrotnych od różnych zespołów, często rozproszonych po całym świecie, wiele firm szuka pomocy w oprogramowaniu do zatwierdzania projektów.
Oto cztery kroki, które pomogą Ci zmienić proces artwork .
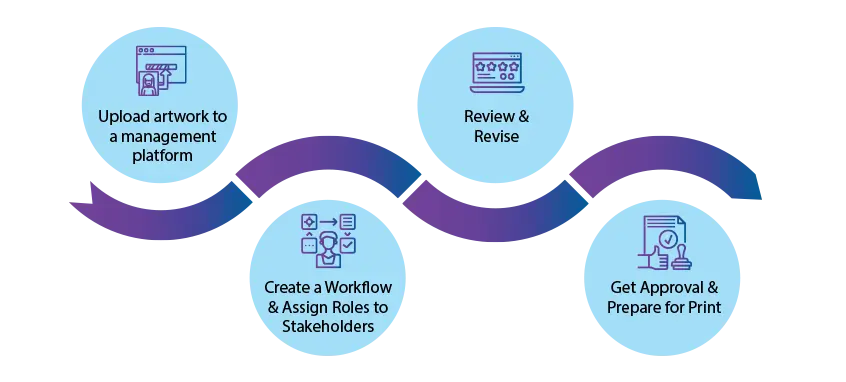
Jakie są oznaki, że Twoja firma potrzebuje dostawcy Artwork ?
Oto kilka kluczowych oznak wskazujących, że Twoja firma może skorzystać na współpracy z dostawcą artwork :
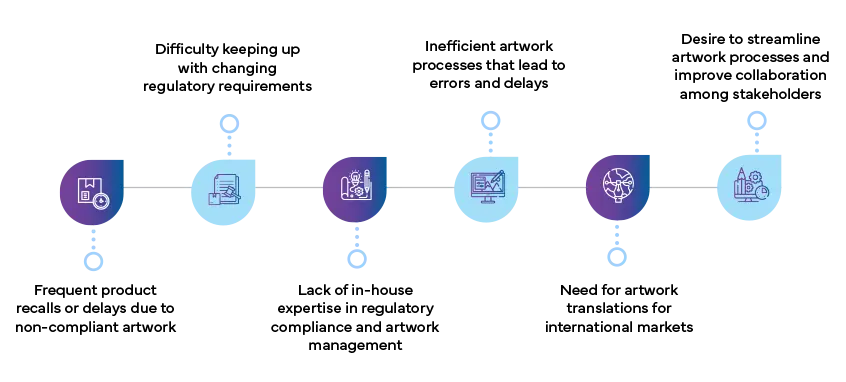
Jakie są korzyści ze współpracy z dostawcą Artwork ?
- Doświadczenie w zakresie zgodności z przepisami: Współpraca z wyspecjalizowanymi dostawcami artwork gwarantuje przestrzeganie rygorystycznych norm regulacyjnych dotyczących etykietowania produktów, opakowań i artwork, co ma kluczowe znaczenie dla zgodności z przepisami prawa i ochrony zdrowia pacjentów.
- Rygorystyczna kontrola jakości: Współpraca z dostawcami artwork gwarantuje skrupulatną dbałość o szczegóły i precyzję, popartą rygorystycznymi środkami kontroli jakości, obejmującymi dokładną korektę, wykrywanie błędów i skrupulatne zarządzanie poprawkami.
- Wykorzystanie zaawansowanych technologii: Wykorzystanie najnowocześniejszych technologii i możliwości automatyzacji, takich jak oprogramowanie do projektowania wspomaganego komputerowo (CAD) i systemy zarządzania treścią (CMS), usprawnia procesy artwork , zwiększając wydajność i skracając czas realizacji.
- Elastyczność i skalowalność: dostawcy Artwork oferują elastyczne i skalowalne rozwiązania, dostosowujące się do różnych artwork pod względem wielkości i złożoności, obsługując zarówno małe, jak i duże projekty.
- Globalna zgodność i lokalizacja: Dzięki doświadczeniu w zarządzaniu artwork dostawcy zapewniają zgodność z wymaganiami językowymi i kulturowymi na różnych rynkach, gwarantując dokładność i spójność komunikatów i treści.
Jak Freyr może ci pomóc na całym świecie?
Freyr wyróżnia się kompleksową ofertą usług regulacyjnych, wspieraną przez zespół ekspertów dobrze zorientowanych w zawiłościach ram regulacyjnych w różnych jurysdykcjach na całym świecie. Dzięki dogłębnej znajomości przepisów takich jak FDA Stanach Zjednoczonych, EMA Europie i różnych organów regulacyjnych w krajach regionu Azji i Pacyfiku, Freyr oferuje dostosowane do indywidualnych potrzeb rozwiązania w zakresie zgodności z przepisami, dostosowane do specyficznych wymagań każdego rynku. Obejmuje to skrupulatne usługi lokalizacyjne, zapewniające dostosowanie artwork do różnych regionów i języków, aby skutecznie dotrzeć do docelowych odbiorców na całym świecie.
Ponadto zaangażowanie firmy Freyr w zapewnienie doskonałości regulacyjnej obejmuje ciągłe monitorowanie zmian i aktualizacji przepisów, umożliwiając klientom pewne poruszanie się po zmieniającym się krajobrazie zgodności z przepisami. Dzięki globalnej sieci biur i partnerów firma Freyr zapewnia płynne wsparcie klientom działającym na różnych rynkach, ułatwiając skuteczne strategie regulacyjne, uzyskiwanie lokalnych zatwierdzeń i artwork . Ponadto firma Freyr priorytetowo traktuje wrażliwość kulturową w artwork , uwzględniając niuanse kulturowe w materiałach, aby zwiększyć akceptację i zaangażowanie lokalnych odbiorców.
- Dogłębna znajomość przepisów: Freyr może pochwalić się zespołem ekspertów ds. regulacji z rozległą wiedzą na temat lokalnych przepisów w różnych regionach. Niezależnie od tego, czy chodzi o FDA w Stanach Zjednoczonych, EMA w Europie, czy organy regulacyjne w krajach Azji i Pacyfiku, nasi eksperci są dobrze zorientowani w zawiłościach każdej jurysdykcji.
- Indywidualne rozwiązania w zakresie zgodności z przepisami: Oferujemy indywidualne rozwiązania w zakresie zgodności z przepisami, dostosowane do konkretnych wymogów regulacyjnych każdego rynku. Wykorzystując naszą lokalną wiedzę specjalistyczną, zapewniamy zgodność artwork , etykiet i opakowań ze wszystkimi obowiązującymi przepisami, ułatwiając płynne wejście na rynek i uzyskanie zatwierdzeń.
- Usługi lokalizacyjne: Freyr świadczy kompleksowe usługi lokalizacyjne w celu dostosowania artwork do różnych regionów i języków. Od tłumaczenia tekstu po dostosowanie obrazów i symboli do preferencji kulturowych — dbamy o to, aby artwork skutecznie artwork do docelowych odbiorców na całym świecie.
- Aktualności dotyczące przepisów prawnych: Nasz zespół na bieżąco monitoruje zmiany i aktualizacje przepisów prawnych w różnych regionach. Wyprzedzając zmieniające się przepisy, pomagamy klientom poruszać się po zmieniającym się krajobrazie zgodności z przepisami i proaktywnie dostosowywać artwork , aby zachować zgodność z przepisami.
- Globalna sieć: Dzięki globalnej sieci biur i partnerów firma Freyr oferuje kompleksowe wsparcie klientom działającym na różnych rynkach. Niezależnie od tego, czy chodzi o opracowanie strategii regulacyjnych, uzyskanie lokalnych zezwoleń czy zarządzanie artwork , nasza lokalna obecność zapewnia wydajną i skuteczną zgodność z przepisami na całym świecie.
- Wrażliwość kulturowa: Rozumiejąc znaczenie wrażliwości kulturowej w artwork , Freyr dba o to, aby materiały klientów trafiały do lokalnych odbiorców. Od preferencji kolorystycznych po wybór obrazów – uwzględniamy niuanse kulturowe w artwork , aby zwiększyć akceptację i zaangażowanie.
Dlaczego Freyr?
Ekspertyza regulacyjna
Ze względu na rygorystyczne normy regulacyjne dotyczące artwork farmaceutycznej, wiedza specjalistyczna w zakresie zgodności z przepisami ma kluczowe znaczenie dla zapewnienia zgodności z prawem i bezpieczeństwa pacjentów.
Partnerstwa strategiczne
Budowanie silnych relacji z klientami sprzyja współpracy i umożliwia tworzenie dopasowanych rozwiązań, które skutecznie odpowiadają na konkretne potrzeby i długoterminowe cele.
Procesy kontroli jakości
Zapewnienie dokładności i precyzji w artwork solidne środki kontroli jakości chroni przed błędami i niezgodnością z przepisami.
Zwinność i elastyczność
W dynamicznym otoczeniu regulacyjnym zdolność do szybkiego dostosowywania się do zmian ma kluczowe znaczenie dla zachowania zgodności i zaspokajania zmieniających się potrzeb klientów.
Kompleksowe usługi
Oferowanie end-to-end artwork usprawnia proces dla klientów, zapewniając wsparcie na każdym etapie, od opracowania koncepcji po ostateczne zatwierdzenie.
Zaawansowana integracja technologii
Wykorzystanie technologii zwiększa wydajność i dokładność artwork , przyczyniając się do skrócenia czasu realizacji i poprawy jakości.
Przejrzysta komunikacja
Otwarta i przejrzysta komunikacja sprzyja zaufaniu i współpracy, zapewniając klientom dostęp do informacji i zaangażowanie w cały proces.
Ciągła innowacja
Innowacje napędzają postęp i zapewniają, że artwork pozostają na najwyższym poziomie, zapewniając klientom optymalne wyniki w nieustannie zmieniającej się branży.
Elastyczność i skalowalność
Zdolność do dostosowania się do zmieniających się wymagań i skalowania operacji w zależności od potrzeb zapewnia, że klienci otrzymują elastyczne i szybko reagujące usługi.
Kompleksowe szkolenia i wsparcie
Wyposażanie klientów w wiedzę i umiejętności umożliwia im niezależne poruszanie się po wymogach regulacyjnych, wspierając samowystarczalność i długoterminowy sukces.
Koncentracja na zrównoważonym rozwoju
Odpowiedzialność środowiskowa jest zgodna z szerszymi wartościami korporacyjnymi i przyczynia się do bardziej zrównoważonej przyszłości, wykazując zaangażowanie w przestrzeganie standardów społecznych i etycznych.
Często zadawane pytania
artwork obejmują tworzenie, zarządzanie i przedkładanie opakowań i etykiet produktów farmaceutycznych zgodnych z globalnymi normami regulacyjnymi. Usługi te obejmują artwork , zgodność etykiet, lokalizację, tłumaczenia, informacje regulacyjne, zarządzanie artwork oraz zapewnienie jakości.
Zasady GMP poprawiają artwork opakowań artwork przejrzystość, dokładność, zarządzanie ryzykiem, identyfikowalność i zgodność z przepisami. Praktyki te ograniczają liczbę błędów, poprawiają wydajność i pozwalają utrzymać reputację marki, zapewniając jednocześnie bezpieczeństwo pacjentów.
Niezgodność może prowadzić do obaw o bezpieczeństwo pacjentów, kar regulacyjnych, utraty reputacji, zobowiązań prawnych, zakłóceń w łańcuchu dostaw, utraty dostępu do rynku, zwiększonej kontroli regulacyjnej i niekorzystnej sytuacji konkurencyjnej. Firmy muszą zachować zgodność z przepisami, aby uniknąć tych zagrożeń.
Automatyzacja artwork usprawnia ten proces, ogranicza liczbę błędów, zapewnia spójność oraz pozwala zaoszczędzić czas i koszty. Zautomatyzowane systemy mogą szybko wykrywać rozbieżności i zapewniać zgodność, poprawiając ogólną jakość i wydajność procesu sprawdzania.
Technologia blockchain to zdecentralizowany, rozproszony system rejestrujący transakcje na wielu komputerach w taki sposób, że zarejestrowane transakcje nie mogą być zmieniane z mocą wsteczną. W kontekście artwork podlegających regulacjom prawnym technologia blockchain może zwiększyć bezpieczeństwo danych i identyfikowalność w całym artwork , promując zaufanie i przejrzystość w ramach regulacji prawnych.
Normy ISO to uznane na całym świecie wytyczne i wymagania, które zapewniają jakość, bezpieczeństwo i wydajność produktów, usług i systemów. W branży farmaceutycznej normy ISO, takie jak ISO 11607 dla opakowań urządzeń medycznych i ISO 13485 dla systemów zarządzania jakością, odgrywają kluczową rolę w utrzymaniu zgodności i zapewnieniu, że opakowania i etykiety spełniają wymogi prawne i bezpieczeństwa.
Projektowanie opakowań odnosi się do procesu tworzenia wizualnych i strukturalnych elementów opakowań produktów, w tym projektowania etykiet, pudełek, butelek i innych formatów opakowań. W branży farmaceutycznej projekt opakowania musi być zgodny z wymogami prawnymi, zapewniając jednocześnie, że wszystkie niezbędne informacje są przekazywane użytkownikom końcowym, w tym instrukcje dotyczące dawkowania, ostrzeżenia i inne istotne szczegóły dotyczące produktu.
Zarządzanie informacjami o produktach (PIM) to system lub proces służący do zarządzania i centralizacji wszystkich danych związanych z produktem, zapewniający wykorzystanie dokładnych i spójnych informacji na różnych platformach i w różnych mediach. W przypadku artwork dotyczących regulacji prawnych PIM pomaga usprawnić proces artwork , zapewniając wykorzystanie najnowszych i najdokładniejszych informacji o produkcie, ograniczając liczbę błędów i poprawiając zgodność z normami regulacyjnymi.











