Przegląd nadzoru po wprowadzeniu do obrotu
Post-market surveillance (PMS) zasadnicze Post-market surveillance (PMS) dla producentów wyrobów medycznych i innych firm zajmujących się dystrybucją wyrobów medycznych, ponieważ zapewnia bezpieczeństwo pacjentów, zgodność wyrobów medycznych z przepisami, ciągłe doskonalenie produktów oraz gwarantuje, że wyroby medyczne bezpieczne, skuteczne i zgodne z przepisami po wprowadzeniu ich do obrotu.
Konsultanci Freyrds. nadzoru po wprowadzeniu do obrotu pomagają producentom urządzeń medycznych w poruszaniu się po zawiłościach przepisów dotyczących nadzoru po wprowadzeniu do obrotu, w tym wymogów nadzoru po wprowadzeniu do obrotu EU MDR i rozpatrywania skarg dotyczących urządzeń medycznych przez FDA .
Usługi nadzoru po wprowadzeniu na rynek
Produkty Zarządzanie reklamacjami
End-to-end zarządzanie End-to-end od momentu ich przyjęcia do zgłoszenia i zamknięcia, zapewniające sprawne, skuteczne i terminowe rozpatrywanie reklamacji w ramach solidnych procesów PMS dotyczących wyrobów medycznych.Zarządzanie wycofywaniem i zwrotami urządzeń
Nasz zespół ekspertów pomoże Ci w poruszaniu się po złożonych przepisach związanych z wycofywaniem urządzeń medycznych i działaniami związanymi z bezpieczeństwem w terenie, zapewniając zgodność, wydajność i minimalne zakłócenia.Korekty i usunięcia
Nasz zespół pomoże w ocenie ryzyka, komunikacji z organami regulacyjnymi i klientami oraz zapewni zgodną z przepisami dokumentację.PMSP, PMSR, PMCF, PSUR, roczna obsługa techniczna
Kompleksowe wsparcie w tworzeniu, aktualizowaniu i utrzymywaniu dokumentacji PMS, w tym planów PMS, raportów PMS, usług PMCF, PSUR oraz corocznych aktualizacji regulacyjnych poprzez fachowy nadzór po wprowadzeniu do obrotu wyroby medyczne.Wielokanałowa i wielojęzyczna obsługa centrum kontaktowego
Nasze dedykowane lokalne oddziały w wielu krajach na całym świecie umożliwią efektywne kosztowo i terminowe wsparcie poprawiające obsługę klienta.Zapytanie i odpowiedź medyczna
Działając jako interfejs między MAH a pacjentem lub konsumentem, nasz zespół zapewni spójne i kontrolowane odpowiedzi na zapytania, stanowiące istotną część nadzoru po wprowadzeniu do obrotu.Ocena zagrożeń dla zdrowia
Przeprowadzamy naukowe, oparte na dowodach oceny w celu oszacowania powagi i prawdopodobieństwa szkód wynikających z wad produktów, tworząc podstawę komunikacji regulacyjnej i podejmowania decyzji dotyczących wycofywania produktów z rynku lub FSCA.Usługa tłumaczenia urządzeń medycznych
Dokładne, zgodne z przepisami tłumaczenie całej dokumentacji związanej z PMS, w tym reklamacji, komunikacji z klientem, FSN, informacji o pacjencie, IFU, etykiet i raportów regulacyjnych, dostarczane przez native speakerów z doświadczeniem w danej dziedzinie.
Usługi nadzoru pozarynkowego Freyr
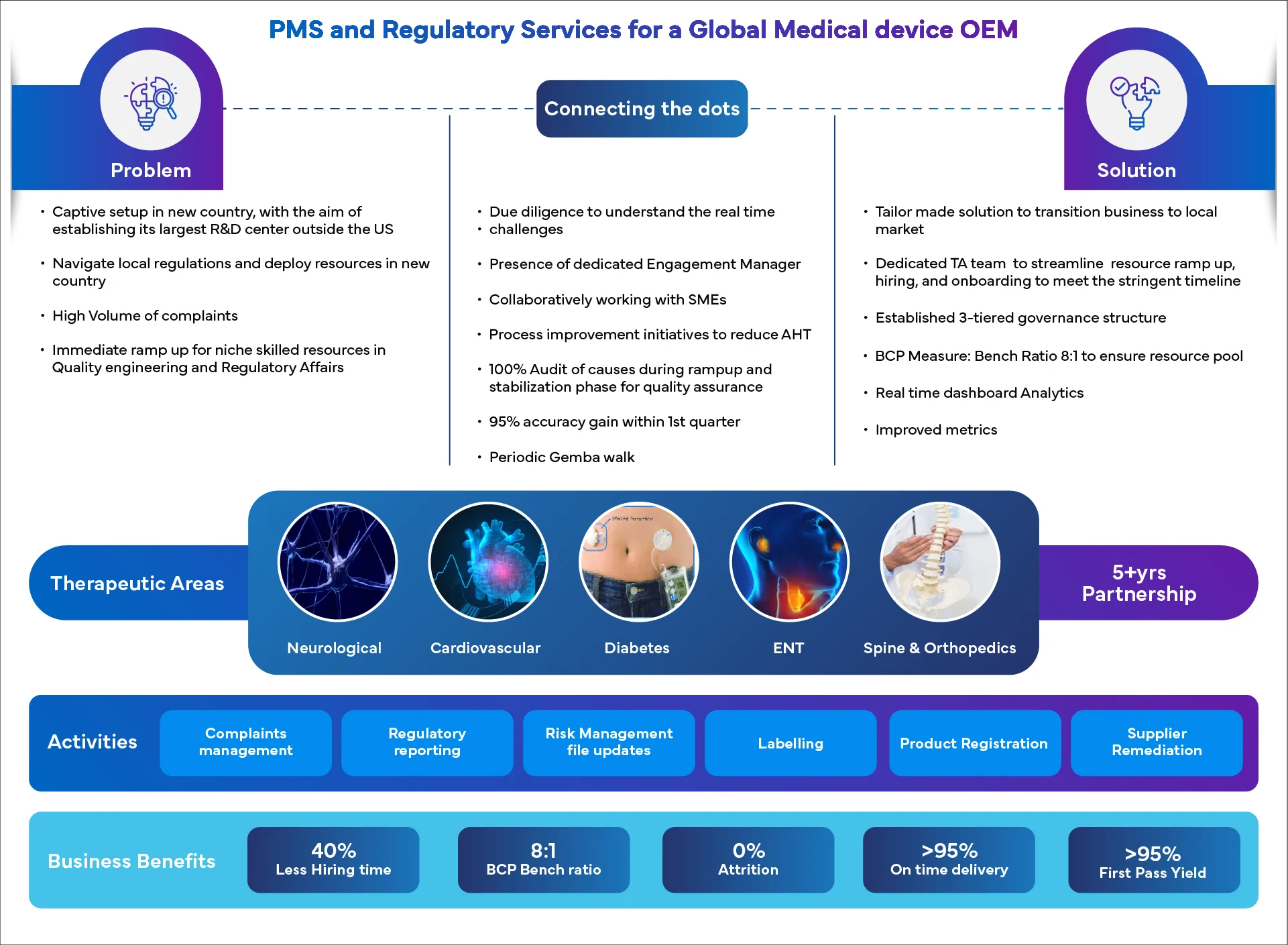
Świętowanie sukcesu klienta
Dlaczego warto współpracować z Freyr?










