
Etykiety leków pełnią rolę przewodnika dla użytkowników i pomagają w jakościowym korzystaniu z produktów. Dlatego bardzo ważne jest, aby informacje dostępne na etykietach były spójne, łatwe do odczytania i wolne od błędów oraz zgodne z globalnymi standardami. Aby dostosować się do tego, Therapeutic Goods Administration (TGA) wprowadziła kilka zmian w sposobie przedstawiania informacji na etykietach produktów. Celem wprowadzenia tych zmian jest poprawa przejrzystości i spójności informacji przekazywanych pracownikom służby zdrowia.
Jakie są nowe zmiany etykiet?
Chociaż nowe informacje są już brane pod uwagę i wdrażane przez producentów, warto je szczegółowo poznać, aby uzyskać kompleksową prezentację. Poniżej wymieniono kilka z nich, nad którymi producenci muszą pracować, definiując swoje etykiety leków.
1. Informacje o składnikach aktywnych
Zgodnie z nową zasadą, aktywne składniki powinny być:
- Umieszczone w bardziej widoczny sposób na przedniej stronie opakowania leku
- Powinna być umieszczona poniżej lub obok nazwy leku na przedniej stronie opakowania.
- Muszą być łatwo porównywalne między lekami
2. Informacje o lekach
Aby zapewnić, że użytkownicy i pracownicy służby zdrowia podejmą świadomą decyzję, informacje o leku powinny być jaśniejsze pod względem:
- Krytyczne informacje zdrowotne na charakterystycznych etykietach
- Wszystkie obowiązkowe informacje muszą być przedstawione w bardziej przejrzysty i rozpoznawalny sposób na tle koloru tła, aby poprawić ich czytelność.
- Substancje podlegające zgłoszeniu, takie jak alergeny, muszą być wymienione na etykiecie.
3. Krytyczne informacje zdrowotne
Krytyczne informacje zdrowotne pomagają konsumentom w bezpiecznym stosowaniu leku, dostarczając ważnych informacji. Informacje zawarte w tabeli krytycznych informacji zdrowotnych będą zawsze w tej samej kolejności, chociaż mogą występować niewielkie różnice w sposobie ich przedstawienia. Krytyczne informacje zdrowotne zawierają następujące nagłówki i informacje w tej samej kolejności:
- Składniki aktywne: Nazwa składnika aktywnego i jego ilość
- Wskazania: Stosowanie leku
- Ostrzeżenia: Zawiera ostrzeżenia, porady i dodatkowe ostrzeżenia dotyczące stosowania leku w części "Wskazówki dotyczące stosowania".
- Instrukcja użycia: Zawiera informacje na temat bezpiecznego stosowania leku.
- Inne informacje: Obejmuje takie informacje, jak szczegóły dotyczące przechowywania, cechy umożliwiające manipulację, dane kontaktowe sponsora, wykaz składników itp. Ta część może nie pojawić się na każdym leku
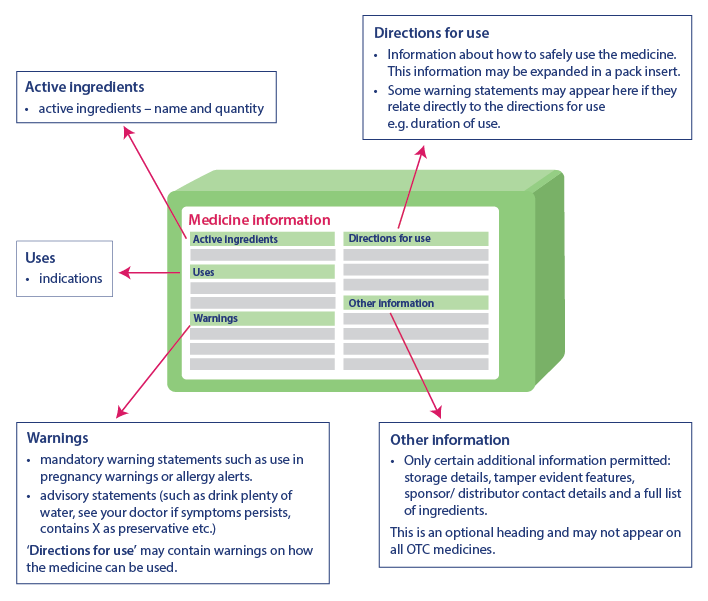
Źródło: TGA
4. Wydawanie leków w aptece
Zgodnie z nową zasadą, następujące zmiany zostały wprowadzone do dozowników leków:
- Aby poprawić identyfikację leków, kartoniki z lekami na receptę muszą zawierać ich nazwę na trzech przeciwległych bokach.
- Etykiety leków na receptę muszą mieć wydzielone miejsce o wymiarach 70 x 30 milimetrów, chyba że są one dostarczane w opakowaniu podstawowym lub startowym.
5. Informacje o alergenach
Leki muszą zawierać następujące informacje na etykietach:
- Jeśli są obecne w leku, wszystkie substancje muszą być zadeklarowane na etykiecie.
- Dodatkowe substancje, takie jak skorupiaki, ryby, jaja, soja, mleko i orzechy, muszą być zadeklarowane na etykiecie.
- W przypadku nowych alergenów, producenci mogą nie uwzględniać ich do końca 4-letniego okresu przejściowego.
Chociaż TGA opublikowało te informacje dla pracowników służby zdrowia, uważamy, że jest to krytyczny wymóg również dla producentów, aby kompleksowo etykietowali swoje produkty. W ten sposób pracownicy służby zdrowia mogą zapoznać się ze zaktualizowanymi informacjami bez żadnych nieporozumień i mogą pokierować pacjentami w celu bezpiecznego spożycia. Powszechnie wiadomo, że TGA zapewniło producentom czteroletni okres przejściowy na wdrożenie tych zmian. Po upływie określonego terminu etykiety leków muszą być zgodne z nowymi wymogami dotyczącymi etykietowania. Bądź na bieżąco. Bądź na bieżąco.









