Servicios de regulación de productos sanitarios
en Singapur Descripción general
En Singapur, los productos sanitarios están regulados por la Ley de Productos Sanitarios (HPA) y su Reglamento de Productos Sanitarios (Productos Sanitarios) de 2010.
Autoridad reguladora: Autoridad de las Ciencias de la Salud (HSA)
Reglamento: Reglamento sobre productos sanitarios de 2010
Vía reglamentaria: Dispositivos Médicos de Dispositivos Médicos de la Autoridad de Ciencias de la Salud (HSA)
Representante autorizado: Singapur Registrante
Requisito del SGC: SS 620:2016, Norma de Singapur sobre buenas prácticas de distribución de productos sanitarios, e ISO 13485:2016.
Evaluación de los datos técnicos: Autoridad de las Ciencias de la Salud (HSA)
Validez de la licencia: Todas las licencias de concesionario son válidas durante 12 meses a partir de la fecha de aprobación
Labelling : Orientaciones reglamentarias, GN- 23 Revisada (1 de marzo de 2020)
Formato de presentación: En línea
Idioma: Inglés
Dispositivos Médicos HSA Dispositivos Médicos
HSA aplica 16 conjuntos de normas para clasificar los productos sanitarios de menor a mayor riesgo en las clases A, B, C y D.
La clasificación del riesgo depende de factores como la duración del contacto, el grado de invasividad, el uso previsto y el método de administración.
Dispositivos Médicos , HSA
| Clase de riesgo | Nivel de riesgo | Dispositivos Médicos |
|---|---|---|
| Clase A | Riesgo bajo | Visor de película, mano quirúrgica, vaina, máscara de oxígeno |
| Clase B | Riesgo de bajo a moderado | Manguito de presión arterial, esterilizador de vástagos |
| Clase C | Riesgo de moderado a alto | Monitor de paciente, mesin Rayos X |
| Clase D | Alto riesgo | Stents cardíacos, marcapasos |
Clasificación IVD
Los productos sanitarios in vitro se clasifican a continuación de menor a mayor riesgo.
Clase de riesgo | Nivel de riesgo | Dispositivos Médicos in vitro |
|---|---|---|
| Clase A | Bajo riesgo individual y bajo riesgo para la salud pública | Recipiente para muestras |
| Clase B | Riesgo individual moderado o bajo riesgo para la salud pública, o ambos | Vitamina B12, autodiagnóstico del embarazo, anticuerpos antinucleares, tiras reactivas de orina |
| Clase C | Riesgo individual elevado o riesgo moderado para la salud pública, o ambos | Autodiagnóstico de glucosa en sangre, tipificación HLA, cribado PSA , Rubéola IgM |
| Clase D | Alto riesgo individual y alto riesgo para la salud pública | Detección del VIH en donantes de sangre, kit de diagnóstico del VIH |
Singapur Representante Dispositivos Médicos /registrado de Dispositivos Médicos
Un registrante es el enlace entre su empresa y HSA, que se encarga del registro de dispositivos en Singapur. El representante Dispositivos Médicos de Singapore Dispositivos Médicos tramita la solicitud de registro ante la HSA es el titular del registro HSA su HSA . Solo las empresas o entidades con sede en Singapur pueden actuar como registrantes; además, deben estar registradas ante la HSA.
Dispositivos Médicos de HSA Dispositivos Médicos
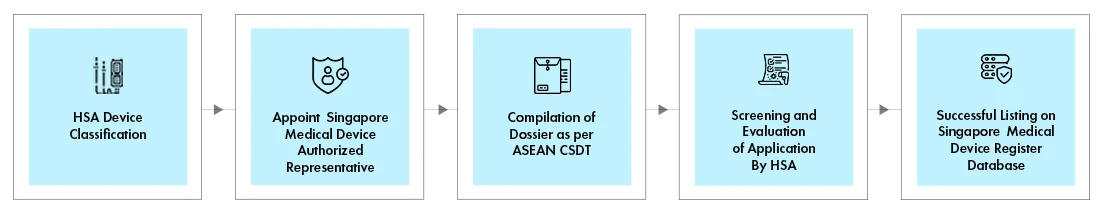
El procesoDispositivos Médicos HSA se lleva a cabo a través del sistema Dispositivos Médicos y Comunicación Dispositivos Médicos (MEDICS) HSA . Cada registro HSA se realiza mediante una vía de evaluación específica, dependiendo de lo siguiente:
- Clasificación del riesgo del dispositivo.
- Número de autorizaciones previas concedidas por los organismos reguladores de referencia en el extranjero.
- Duración del historial de comercialización segura del dispositivo.
La ruta de evaluación del dispositivo determinará el plazo de entrega (TAT), las tasas y los documentos necesarios para el registro.
Registro de Clase A - Los productos sanitarios de Clase A están exentos del registro de productos. Sin embargo, es necesario cumplimentar la lista de exención de clase A en MEDICS durante la solicitud de licencia del distribuidor.
Flujo del proceso
Gestión del ciclo de vida de los dispositivos tras su aprobación
Freyr presta apoyo a fabricantes extranjeros en la gestión end-to-end Dispositivos Médicos , incluidas las actividades posteriores a la autorización, tales como:
- Gestión de cambios posteriores a la aprobación: modificaciones de Dispositivos Médicos existentes Dispositivos Médicos , como la incorporación de nuevas variantes y accesorios, la incorporación de nuevas indicaciones de uso, entre otras.
- Mantenimiento de Dispositivos Médicos y registros Dispositivos Médicos mediante el pago puntual de las tasas administrativas y de registro.
- Renovación de la licencia.
Con un equipo profesional que proporciona apoyo normativo, Freyr ayuda a los fabricantes a mantener la calidad y seguridad necesarias para la aprobación. Los expertos en inteligencia de Freyrobservan atentamente las actualizaciones normativas e informan a los clientes sobre los pasos que deben dar para que sus productos cumplan las normas vigentes.
Resumen
El plazo de tramitación del registro de productos se indica en el cuadro siguiente.
| Clase de riesgo | Inmediato | Acelerado | Abridged | Evaluación completa | Pleno (Sistema de examen prioritario) |
|---|---|---|---|---|---|
| Clase B | Registro inmediato tras la presentación | 100 días laborables | 160 días laborables | 120 días laborables | |
| Clase C | Registro inmediato tras la presentación (sólo para aplicaciones móviles médicas independientes de clase C) | 120 días laborables | 160 días laborables | 220 días laborables | 165 días laborables |
| Clase D | 180 días laborables | 220 días laborables | 310 días laborables | 235 días laborables | |
| Clase D (dispositivos que incorporan productos medicinales) | 220 días laborables | 310 días laborables |
El plazo de tramitación de un cambio de registrante es de 40 días laborables.
NOTA-
- Los productos sanitarios de clase A están exentos del registro de productos.
- El plazo de entrega excluye el tiempo necesario para responder a cualquier solicitud de aclaración o información adicional por parte de HSA durante la fase de evaluación.
Experiencia Freyr
- Diligencia debida reglamentaria para el registro de dispositivos en la HSA, Singapur
- Dispositivos Médicos y agrupación de HSA Dispositivos Médicos
- Apoyo a la evaluación del organismo de evaluación de la conformidad (OEC)
- ASEAN Common Submission Dossier Template (CSDT) Compilación de expedientes
- Registro de dispositivos HSA ;
- Representación jurídica
- Apoyo al etiquetado
- Identificación y cualificación de distribuidores
- Vigilancia posterior a la comercialización
- Gestión de cambios posterior a la aprobación
- Renovación y transferencia de licencias
- Servicios de presentación y enlace con la HSA