Informe de Validez Científica (IVE)
El Informe de Validez Científica (SVR, por sus siglas en inglés) tiene una importancia primordial dentro del Informe de Evaluación de Funcionamiento (PER, por sus siglas en inglés) para Dispositivos de Diagnóstico In Vitro (IVD, por sus siglas en inglés), según el Reglamento de Diagnóstico In Vitro de la Unión Europea (EU IVDR) 2017/746. El SVR desempeña un papel crucial en la validación científica del rendimiento analítico y clínico del dispositivo, garantizando la seguridad y la eficacia de los dispositivos médicos disponibles en el mercado. En el marco del proceso de evaluación de la conformidad prescrito por el Reglamento de diagnóstico in vitro de la UE, los fabricantes deben presentar un PER, que debe incluir un SVR, a un organismo notificado para demostrar la seguridad y el rendimiento del producto antes de su introducción en el mercado de la UE.
Informes de validez científica para la presentación de IVDR en la UE
- Análisis y conclusiones
¿Cuál es el contenido del Informe de Validez Científica (IVE)?
Por validez científica de un analito se entiende la asociación de un analito con una condición clínica o un estado fisiológico. La validez científica de un DIV se basa principalmente en una de las siguientes fuentes o en una combinación de ellas:
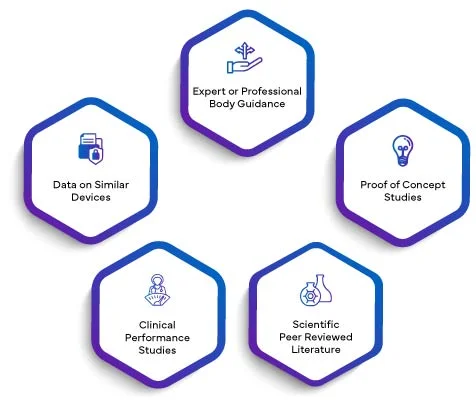
Los datos de todo lo anterior, según proceda, se redactarán en un informe de validez científica. Al integrar el SVR en el PER, los fabricantes elevan su evaluación del rendimiento a un nivel superior de credibilidad. La validez científica establecida mediante el SVR infunde al PER una base sólida, mejorando su calidad e importancia generales. Esto, a su vez, infunde confianza en los organismos reguladores, los profesionales sanitarios y los usuarios finales, garantizando que el rendimiento del DIV se evalúa y valida meticulosamente de acuerdo con los estrictos requisitos del IVDR 2017/746 de la UE.
Freyr ofrece asistencia completa en la preparación de un sólido Informe de Validez Científica (SVR) para IVDs, permitiéndole navegar con confianza por el panorama regulatorio e introducir sin problemas en el mercado dispositivos IVD seguros y eficaces.
Informe de validez científica
- Plan de transición para el cumplimiento del IVDR.
- Informe de Validez Científica (SVR) basado en la bibliografía y/o en datos internos.
- Informes de rendimiento clínico (RCP) basados en la bibliografía y/o en datos internos.
- Informes analíticos de resultados (IAA)
- Pruebas clínicas o informes de evaluación del rendimiento según el IVDR.
- Plan de evaluación del rendimiento.
- Protocolos e informes de seguimiento de los resultados del mercado.
- Protocolos e informes de vigilancia postcomercialización (PMSR).
- Redacción/Revisión de otros documentos, como el prospecto/IFU, las instrucciones de referencia rápida (QRI), el manual de funcionamiento/usuario, etc.

- Cumplimiento garantizado de la normativa aplicable reciente.
- Equipo de expertos cualificados
- Soluciones adaptadas a sus necesidades
- Gestión de recursos reglamentarios/Servicios de aumento de personal
- Aportaciones interfuncionales de Dispositivos Médicos para cumplir con los requisitos.