
Los productos combinados o los productos que combinan medicamentos, dispositivos o productos biológicos plantean problemas especiales de etiquetado reglamentario. Como estos productos constan de múltiples componentes y normas reglamentarias diferentes, los fabricantes deben asegurarse de que cumplen todos los requisitos individuales y transmiten adecuadamente la información de seguridad.
Este blog explora los retos del etiquetado de productos combinados y proporciona estrategias para navegar por los requisitos reglamentarios de etiquetado, al tiempo que prioriza la seguridad del paciente y el cumplimiento. La figura 1 destaca los principales retos del etiquetado de productos combinados.
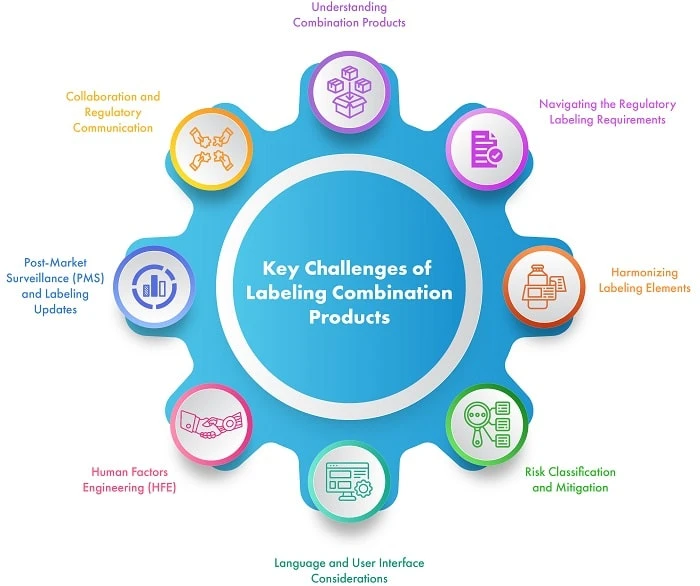
Figura 1: Principales retos del etiquetado de productos combinados
Veamos us cada reto en detalle:
- Productos combinados: Los productos combinados combinan varios componentes, por ejemplo, un producto formado por un fármaco y un dispositivo, para ofrecer opciones de tratamiento innovadoras. Sin embargo, la convergencia de diferentes marcos y requisitos normativos puede complicar su proceso de etiquetado. Por lo tanto, es fundamental reconocer el método fundamental de funcionamiento y la normativa pertinente para cada componente.
- Cumplimiento de los requisitos normativos de etiquetado: los productos combinados deben cumplir tanto la legislación sobre medicamentos como la relativa a los dispositivos médicos, lo que hace necesario cumplir múltiples vías normativas. Colabore estrechamente con Asuntos Regulatorios para comprender y abordar los requisitos específicos de etiquetado establecidos por organismos como la Administración de Alimentos y Medicamentos de los Estados Unidos (USFDA), la Agencia Europea de Medicamentos (EMA) y otras autoridades pertinentes.
- Armonización de los elementos de etiquetado: La armonización de los elementos de etiquetado entre los diferentes componentes de los productos combinados es crucial para proporcionar información clara y coherente a los profesionales sanitarios y a los pacientes. Asegúrese de que el etiquetado represente con precisión la funcionalidad combinada y transmita las instrucciones, advertencias e instrucciones de uso (IFU) esenciales.
- Clasificación y mitigación de riesgos: Identificar y clasificar los riesgos asociados a cada componente del producto combinado. Evaluar los riesgos potenciales y determinar las estrategias de mitigación apropiadas. Comunicar estos riesgos, junto con las precauciones y advertencias correspondientes en la etiqueta del producto, para garantizar la seguridad del paciente y el cumplimiento de los requisitos reglamentarios de etiquetado.
- Consideraciones sobre el idioma y la interfaz de usuario: Tenga en cuenta los requisitos lingüísticos del etiquetado cuando comercialice productos combinados a escala internacional. Traduzca y localice el contenido del etiquetado para que cumpla la normativa de las distintas regiones y se adapte a las preferencias lingüísticas del público destinatario. Además, diseñe interfaces fáciles de usar que faciliten el uso seguro y eficaz de los productos combinados.
- Ingeniería de los factores humanos (HFE): La facilidad de uso de los productos combinados es fundamental para garantizar la seguridad del paciente. Aplique los principios de HFE para garantizar que el etiquetado y las instrucciones de uso sean intuitivos, fácilmente comprensibles y compatibles con la interfaz de usuario del componente del dispositivo. Realice pruebas de usabilidad y repita el diseño para reducir el riesgo de errores y optimizar la experiencia del usuario.
- Post-market Surveillance (PMS) actualizaciones del etiquetado: Supervisar continuamente la seguridad y el rendimiento de los productos combinados a través de la PMS. Capturar y analizar rápidamente los eventos adversos y las preocupaciones emergentes en materia de seguridad. Actualizar el etiquetado, cuando sea necesario, para reflejar cualquier nueva información, advertencia de seguridad o cambio en las indicaciones.
- Colaboración y comunicación reglamentaria: El etiquetado de productos combinados requiere una estrecha colaboración entre los equipos de regulación, calidad y marketing. Establezca canales de comunicación eficaces con las autoridades reguladoras para buscar orientación, aclarar los requisitos y garantizar el cumplimiento durante todo el proceso de etiquetado. Aproveche la experiencia de los equipos interfuncionales para desarrollar un etiquetado completo y conforme.
Conclusión
El etiquetado de productos combinados implica navegar por marcos normativos complejos, abordar la clasificación de riesgos y garantizar una comunicación eficaz de la información de seguridad. Al comprender los desafíos únicos, armonizar los elementos de etiquetado y aprovechar la experiencia regulatoria, los fabricantes pueden manejar los desafíos con facilidad y priorizar el cumplimiento y la seguridad del paciente.
Preste mucha atención a los requisitos normativos y etiquete con precisión sus productos combinados, para que los profesionales sanitarios y los pacientes puedan utilizarlos de forma segura y eficaz. Asociarse con un experto como Freyr minimizar sus esfuerzos. ¡Póngase en contacto con us para obtener más información.









