
Audyty dobrych praktyk wytwarzania (GMP) i dobrych praktyk dystrybucji (GDP) mają kluczowe znaczenie dla zapewnienia jakości, bezpieczeństwa i integralności produktów farmaceutycznych w całym cyklu ich życia. Przeprowadzanie dokładnych badań podczas tych audytów jest niezbędne do identyfikacji i usuwania wszelkich odchyleń, niezgodności lub potencjalnych zagrożeń. W tym wpisie na blogu omówimy znaczenie dogłębnych badań podczasGDP i przedstawimy cenne informacje na temat przeprowadzania skutecznych badań w celu zapewnienia zgodności z przepisami.
Zrozumienie znaczenia szczegółowych dochodzeń
- Identyfikacja przyczyn źródłowych: Dogłębne badania pomagają odkryć podstawowe przyczyny odchyleń lub niezgodności, umożliwiając firmom zajęcie się przyczynami źródłowymi, a nie tylko leczeniem objawów.
- Zapobieganie nawrotom: Dzięki zrozumieniu przyczyn źródłowych, firmy mogą wdrożyć działania naprawcze i zapobiegawcze (CAPA), aby zapobiec powtarzaniu się podobnych problemów w przyszłości, poprawiając w ten sposób ogólną zgodność i jakość produktów.
- Zapewnienie bezpieczeństwa produktu: Dokładne badania zapewniają, że wszelkie potencjalne zagrożenia dla bezpieczeństwa lub skuteczności produktu są szybko identyfikowane i łagodzone, chroniąc zdrowie i dobrostan pacjentów.
- Zachowanie zgodności z przepisami: Organy regulacyjne oczekują od firm przeprowadzania dokładnych dochodzeń w sprawieGDP oraz podejmowania odpowiednich działań naprawczych w celu zachowania zgodności z normami regulacyjnymi.
Kluczowe kroki w prowadzeniu szczegółowych dochodzeń:
- Przegląd dokumentacji: Rozpocznij od przejrzenia odpowiedniej dokumentacji, w tym standard operating procedures (SOPs), dokumentacji partii, raportów dotyczących odchyleń i wyników poprzednich audytów, aby uzyskać wgląd w daną kwestię.
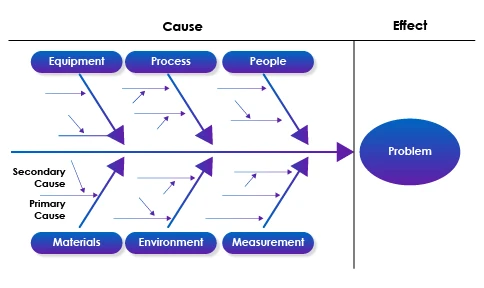
- Analiza przyczyn źródłowych: Korzystanie z narzędzi i metodologii, takich jak 5 powodów, diagramy Fishbone (Ishikawa) lub analiza przyczyn i skutków awarii (FMEA) w celu systematycznego identyfikowania pierwotnych przyczyn odchyleń lub niezgodności.
Diagram rybiej ości jako przykład
- Gromadzenie danych: Zbieranie odpowiednich danych i dowodów poprzez wywiady, obserwacje i analizę danych w celu wsparcia ustaleń i wniosków z dochodzenia.
- Współpraca międzyfunkcyjna: W procesie dochodzeniowym należy zaangażować zespoły międzyfunkcyjne, w tym zespoły ds. zapewnienia jakości, produkcji, łańcucha dostaw i Sprawy regulacyjne, aby zapewnić kompleksowe zrozumienie problemu i ułatwić skuteczne rozwiązywanie problemów.
- Działania naprawcze i zapobiegawcze (CAPA): Opracowanie i wdrożenie działań naprawczych i zapobiegawczych (CAPA) w oparciu o wyniki dochodzenia w celu wyeliminowania przyczyn źródłowych i zapobieżenia powtórzeniu się podobnych problemów w przyszłości.
- Ciągłe doskonalenie: Wykorzystanie spostrzeżeń uzyskanych w wyniku dochodzeń do prowadzenia inicjatyw ciągłego doskonalenia, takich jak optymalizacja procesów, programy szkoleniowe lub aktualizacje technologii, w celu poprawy ogólnej jakości i zgodności.
Wnioski:
Przeprowadzanie dogłębnych dochodzeń podczasGDP ma zasadnicze znaczenie dla utrzymania zgodności z przepisami, zapewnienia jakości produktów i ochrony bezpieczeństwa pacjentów. Dzięki systematycznym procesom dochodzeniowym, identyfikacji przyczyn źródłowych oraz wdrażaniu skutecznych działań naprawczych i zapobiegawczych firmy mogą wzmocnić swoje systemy zarządzania jakością i wykazać swoje zaangażowanie w przestrzeganie przepisów oraz ciągłe doskonalenie. Skuteczne dochodzenia nie tylko ograniczają ryzyko, ale także przyczyniają się do budowania kultury jakości i doskonałości w organizacji.









