
System informacji o badaniach klinicznych (CTIS) to scentralizowana baza danych, która wspiera prowadzenie badań klinicznych w Unii Europejskiej (UE). Został uruchomiony w styczniu 2022 r. i stanowi kluczowy element rozporządzenia w sprawie badań klinicznych (CTR), którego celem jest poprawa efektywności i przejrzystości badań klinicznych w UE. CTIS szereg funkcji, które sprawiają, że jest cennym narzędziem dla sponsorów badań klinicznych, naukowców i organów regulacyjnych.
Funkcje te obejmują:
- Pojedynczy punkt wejścia do zgłaszania i zarządzania badaniami klinicznymi w wielu krajach.
- Bezpieczny i wydajny sposób wymiany informacji między sponsorami, badaczami i organami regulacyjnymi.
- Publicznie dostępna baza danych badań klinicznych z możliwością wyszukiwania.
- Narzędzia wspierające monitorowanie i nadzorowanie badań klinicznych.
- CTIS już teraz CTIS pozytywny wpływ na sytuację w zakresie badań klinicznych w UE. Ułatwia i przyspiesza przeprowadzanie badań klinicznych oraz zapewnia większą przejrzystość i dostępność danych z badań klinicznych.
Poznaj CTIS dla badań klinicznych
Zoptymalizuj swoje badania kliniczne już teraz
Jak CTIS krajobraz badań klinicznych:
- CTIS przeprowadzanie badań klinicznych w wielu krajach:
Wcześniej sponsorzy musieli składać osobne wnioski do każdego kraju, w którym chcieli przeprowadzić badanie kliniczne. Był to proces czasochłonny i kosztowny. CTIS sponsorom złożenie jednego wniosku, który jest ważny we wszystkich Member States UE. Dzięki temu sponsorzy mogą znacznie łatwiej i szybciej przeprowadzać badania kliniczne w wielu krajach.
- CTIS efektywność procesu oceny badań klinicznych:
Organy regulacyjne w różnych krajach mogą teraz łatwiej współpracować dzięki CTIS. Oznacza to, że wnioski mogą być rozpatrywane szybciej i skuteczniej.
- CTIS przejrzystość danych dotyczących badań klinicznych:
Publiczna strona internetowa CTIS dostęp do informacji o wszystkich badaniach klinicznych zarejestrowanych w systemie. Informacje te obejmują protokół badania, wyniki badania oraz wszelkie kwestie związane z bezpieczeństwem. Ta zwiększona przejrzystość pomaga budować zaufanie społeczne do badań klinicznych.
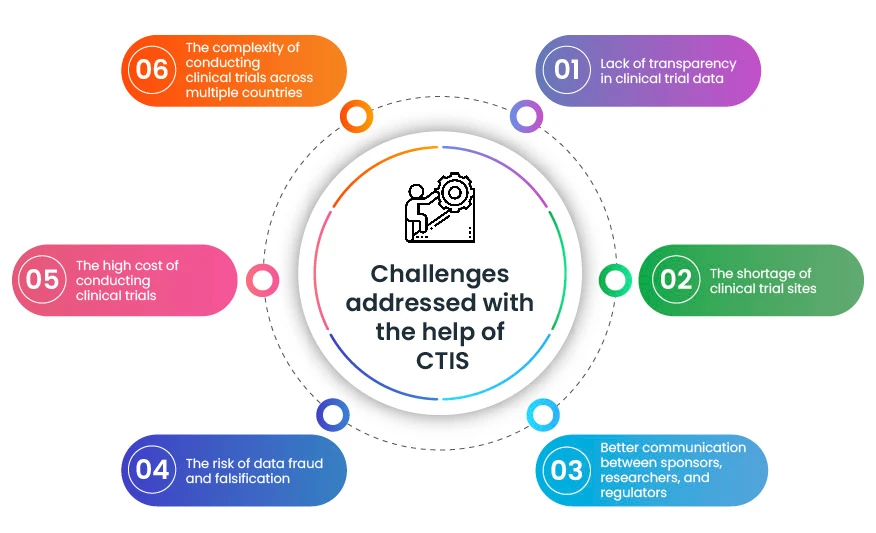
CTIS cenne narzędzie, które pomaga w pokonywaniu niektórych kluczowych wyzwań pojawiających się podczas badań klinicznych. Dzięki ułatwieniu, przyspieszeniu i zwiększeniu przejrzystości przeprowadzania badań klinicznych, CTIS szybkie wprowadzanie nowych metod leczenia dla pacjentów.
CTIS wciąż stosunkowo nowym systemem, ale ma potencjał, aby zrewolucjonizować sposób prowadzenia badań klinicznych w UE. W świecie, w którym postęp naukowy ma większe znaczenie niż kiedykolwiek, CTIS, w synergii z globalnym partnerem regulacyjnym, takim jak Freyr, ma kluczowe znaczenie dla otwierania nowych horyzontów w dziedzinie opieki zdrowotnej. Wdrażając te przełomowe technologie, torujemy drogę do szybszych, bezpieczniejszych i bardziej znaczących odkryć, które mogą kształtować przyszłość medycyny dla przyszłych pokoleń.









