
Reklama produktów farmaceutycznych, w tym reklama skierowana bezpośrednio do konsumentów, jest regulowana odpowiednio przez Biuro Promocji Leków na Receptę (OPDP) Amerykańskiej Agencji ds. Żywności i Leków (US FDA), Oddział ds. Reklamy i Etykiet Promocyjnych (APLB) w Centrum Oceny i Badań Leków (CDER) oraz Centrum Oceny i Badań Produktów Biologicznych (CBER). Informacje przekazywane do OPDP i APLB być dokładne, etyczne i nie mogą wprowadzać w błąd. W zgłoszeniu należy zawrzeć dodatkowe informacje na temat korzyści i zagrożeń związanych z produktem. Urzędy te sprawdzają również materiały promocyjne przekazywane do Agencji.
W kwietniu 2022 r. US agencjaFDA wytyczne dotyczące składania materiałów promocyjnych i reklamowych. Wytyczne pomagają w zrozumieniu procesu składania wniosków elektronicznych w module 1 eCTD przy użyciu pliku US w wersji 3.3 lub wyższej. W dokumencie wymieniono rodzaje materiałów promocyjnych, które nie podlegają obowiązkowi składania wniosków elektronicznych zgodnie z sekcją 745A. Papierowe kopie wszystkich rodzajów wniosków promocyjnych będą przyjmowane przez dwadzieścia cztery (24) miesiące od daty publication wytycznych.
Wyjątek
W dokumencie stwierdza się, że wnioski składane na podstawie sekcji 505(b), (i) lub (j) federalnej ustawy o żywności, lekach i kosmetykach (FD&C Act) oraz wnioski składane na podstawie sekcji 47 351(a) lub (k) ustawy o służbie zdrowia publicznego (PHS Act) muszą być składane w formacie elektronicznym określonym przez FDA. Niniejszy dokument nie podlega zwykłym ograniczeniom zawartym w przepisach FDAdobrych praktyk w zakresie wytycznych, ponieważ nie został ustanowiony prawnie w celu egzekwowania obowiązków. W związku z tym część niniejszych wytycznych, która ustanawia wymóg składania wniosków w formie elektronicznej zgodnie z sekcją 745A(a) ustawy FD&C, ma charakter wiążący, co wskazuje użycie słów „musi”, „powinien” lub „wymagane”.
FDA przygotowanych materiałów promocyjnych w ciągu czterdziestu pięciu (45) dni od dobrowolnego przedłożenia ich przez sponsorów. W przypadku wszelkich pytań dotyczących produktu zgłaszanych przez pracowników służby zdrowia, konsumentów, sponsorów leków lub kancelarie prawne, OPDP przyznaje sponsorom prawo do udzielenia odpowiedzi w ciągu trzydziestu (30) dni kalendarzowych.
Definicja materiałów promocyjnych
Termin „materiały promocyjne” odnosi się do etykiet promocyjnych i materiałów reklamowych, niezależnie od formatu, sposobu lub nośnika, za pomocą którego są one przekazywane. FDA nadzoruje FDA dwa (02) rodzaje etykietowania leków:
- Etykietowanie FDA
- Etykiety promocyjne
Zgodnie z sekcją 201(m) FDA, etykietowanie definiuje się jako „wszystkie etykiety oprócz napisów, nadruków lub grafik wytłoczonych na dowolnym pojemniku, opakowaniu lub dowolnym artykule lub towarzyszącym takiemu artykułowi”. Sformułowanie „towarzyszący takiemu artykułowi” jest traktowane jako interpretacja lub wyjaśnienie materiału promocyjnego, zgodnie z orzeczeniem Sądu US
Kryteria zgłaszania materiałów promocyjnych do przeglądu
- Włączenie odpowiednich BLA NDA, ANDA lub BLA
- W przypadkach, w których wnioskodawcy wymagają natychmiastowego przeglądu, należy kierować zgłoszenia do Kierownika Projektu OPDP
- Z formularza FDA wybierz najbardziej szczegółowy rodzaj materiału, który reprezentuje materiał promocyjny.
- Różne rodzaje materiałów należy przesyłać oddzielnie
- Nie mieszaj innych zgłoszeń z materiałami promocyjnymi
- Materiały promocyjne skierowane do pracowników służby zdrowia muszą być składane oddzielnie od tych skierowanych do konsumentów.
Poniższe metryki wyjaśniają liczbę przesłanych formularzy 2253 i materiałów zawartych w tych zgłoszeniach.
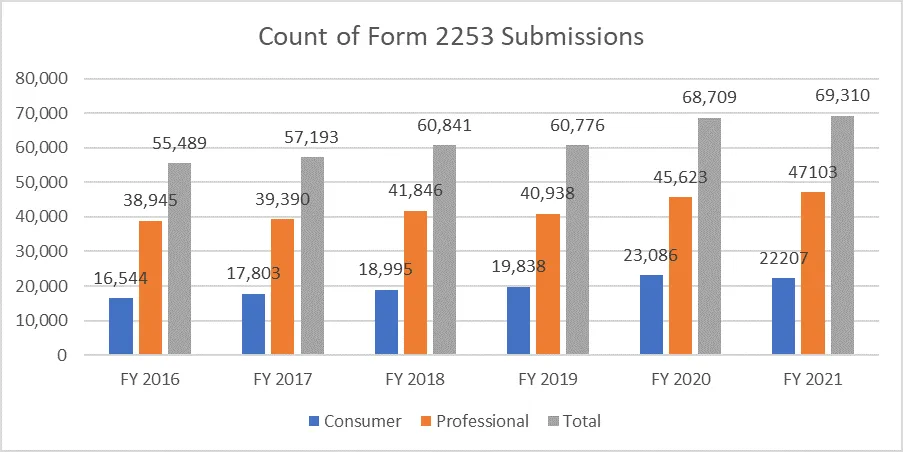
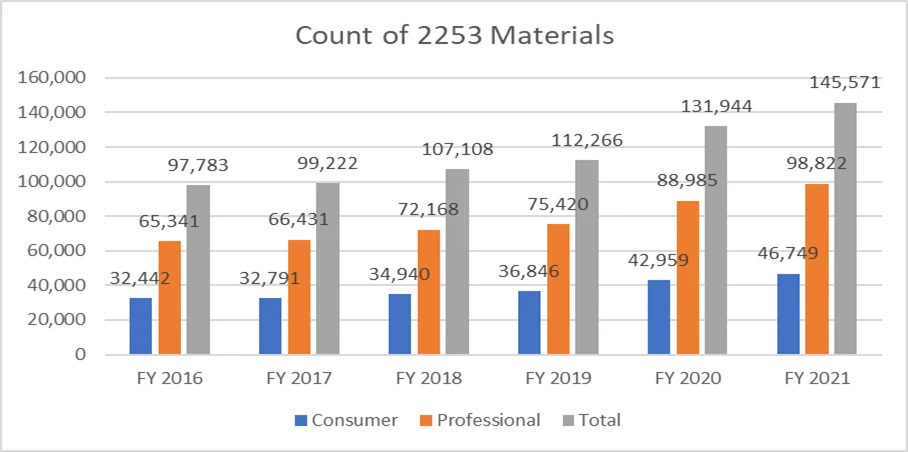
Ze względu na koszty procesu niezwykle ważne jest, aby sponsorzy opracowywali materiały promocyjne zgodnie z wytycznymi FDA uniknąć wielokrotnych cykli przeglądu. Posiadanie zasobów, które mogą pomóc w płynnym przebiegu procesu składania materiałów promocyjnych, umożliwia sponsorom osiągnięcie celów biznesowych i zachowanie zgodności z wymogami regulacyjnymi. Sprawdzony partner regulacyjny, taki jak Freyr zapewnić kompletny przegląd materiałów promocyjnych i niepromocyjnych przed ich złożeniem, zarówno w formacie elektronicznym, jak i nieelektronicznym. Skontaktuj się z Freyr już dziś, aby od razu przygotować jasne, zwięzłe i zgodne z przepisami materiały promocyjne.









