En el panorama en constante evolución del desarrollo farmacéutico, el camino desde el descubrimiento en el laboratorio hasta el tratamiento del paciente está plagado de complejos retos normativos. En este proceso se encuentra la solicitud de nuevo fármaco (NDA), un hito fundamental que abarca el esfuerzo científico y la inversión. Este blog profundiza en las complejidades de las operaciones NDA , ofreciendo valiosas ideas y lecciones aprendidas de veteranos del sector.
NDA
Las solicitudes de nuevos medicamentos representan la culminación de una exhaustiva labor de investigación, desarrollo y ensayos clínicos. Constituyen un expediente completo que convence a las autoridades reguladoras, como la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA), de que un nuevo medicamento es seguro, eficaz y está listo para su aprobación comercial.
La complejidad del NDA de NDA
Uno de los principales obstáculos en NDA es el gran volumen y la complejidad de los datos requeridos. Las empresas farmacéuticas deben sortear un laberinto de directrices reglamentarias al tiempo que presentan pruebas claras y convincentes de las ventajas de sus medicamentos. Este equilibrio a menudo provoca retrasos, costosas revisiones y, en algunos casos, rechazos directos.
Para arrojar luz sobre este proceso crítico, analicemos las etapas clave de NDA y exploremos estrategias para tener éxito en cada paso.
Tabla 1: Etapas clave en NDA )
| Escenario | Descripción | Buenas prácticas |
|---|---|---|
| Investigación preclínica | Estudios de laboratorio y con animales para recopilar datos iniciales | Garantizar un diseño sólido del estudio y una recopilación meticulosa de los datos. |
| Ensayos clínicos | Ensayos en humanos realizados en fases (I, II, III) | Aplicar protocolos rigurosos y mantener la integridad de los datos |
| Documentación | Recopilación de datos sobre seguridad, eficacia y calidad | Organizar los datos sistemáticamente y garantizar la claridad de la presentación. |
| Revisión de la normativa | Presentación ante FDA proceso de revisión | Mantener una comunicación abierta con los organismos reguladores |
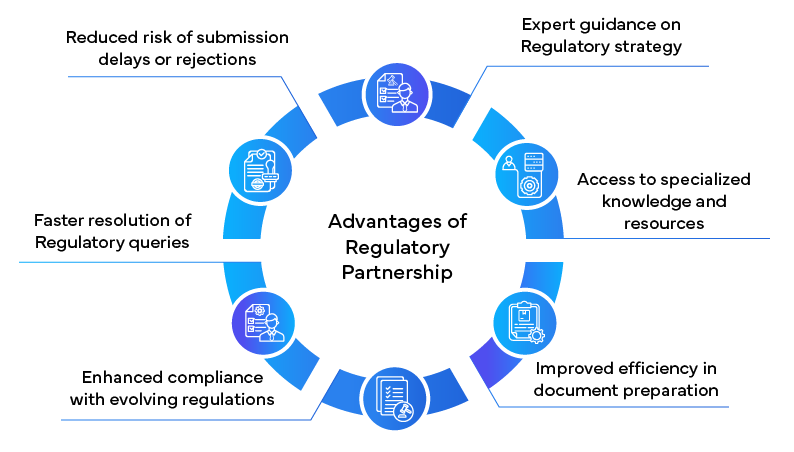
Papel de la asociación reguladora
A la hora de navegar por el complejo NDA , muchas empresas farmacéuticas están recurriendo a socios reguladores en busca de apoyo. Estas empresas especializadas ofrecen una gran experiencia y conocimientos que pueden agilizar considerablemente el NDA .
Lecciones aprendidas
De cara al futuro, la importancia de unas operaciones NDA eficaces en materia de NDA no hará más que aumentar. Con la aceleración del ritmo de la innovación y la evolución del panorama regulador, quienes dominen este proceso crítico estarán en la mejor posición para ofrecer tratamientos que cambian la vida de los pacientes de todo el mundo.
El camino hacia una NDA exitosa NDA rara vez es sencillo; sin embargo, al adoptar un enfoque estratégico para las operaciones regulatorias, aprovechar las asociaciones con expertos y mantener un compromiso con la calidad y el cumplimiento, las empresas farmacéuticas pueden mejorar significativamente sus posibilidades de NDA .