
Le 27 mai 2016, la Food and Drug Administration (FDAUS a publié dans le Federal Register la version définitive de la réglementation relative à l'étiquetage nutritionnel et des compléments alimentaires. Cette réglementation garantit que l'étiquetage reflète les nouvelles données scientifiques, notamment le lien entre l'alimentation et les maladies chroniques telles que l'obésité et les maladies cardiaques. La nouvelle réglementation vise à garantir que l'étiquetage des produits soit conforme aux habitudes et pratiques alimentaires actuelles, qui n'étaient pas clairement établies dans l'ancienne réglementation. Une autre mise à jour importante de la règle est que la FDA fixé des délais de mise en conformité en fonction du chiffre d'affaires annuel de l'organisation dans le domaine alimentaire.
Délais de mise en conformité
Les fabricants de nutraceutiques qui souhaitent entrer sur le marché américain doivent se conformer à la nouvelle règle d'étiquetage dans les délais impartis, faute de quoi ils s'exposent à des rappels de produits. Les délais sont les suivants :
- 1er janvier 2020 pour les fabricants dont le chiffre d'affaires annuel est supérieur ou égal à 10 millions de dollars
- 1er janvier 2021 pour les fabricants dont le chiffre d'affaires annuel est inférieur à 10 millions de dollars
Voulez-vous entrer sur le marché américain ? Évaluez vos procédures réglementaires.
Principaux changements apportés à l'étiquetage nutritionnel
Pour se conformer à la nouvelle règle, les parties prenantes doivent décoder la règle révisée et s'y conformer en conséquence. La règle révisée comprend, sans s'y limiter, les changements énumérés ci-dessous.
- Éliminer les déclarations de "calories provenant des graisses".
- Assurer la déclaration des grammes (g) de "sucres ajoutés" dans une portion du produit.
- Établir la valeur journalière de référence (VJR) pour les sucres ajoutés et déclarer le pourcentage de la valeur journalière (VJ) pour ces mêmes sucres.
- Remplacer "Sucres" par "Sucres totaux" et déclarer "Dont 'X' grammes de sucres ajoutés" directement sous "Sucres totaux".
- Mise à jour de la liste des vitamines et minéraux présentant un intérêt du point de vue de la santé publique
- Mise à jour des valeurs de référence utilisées dans la déclaration des VQ actuelles des nutriments sur les étiquettes de la valeur nutritive
- Réviser le format des étiquettes de la valeur nutritive afin de mettre davantage en évidence la mention "Calories".
- Suppression de l'exigence d'un tableau de notes de bas de page énumérant les valeurs de référence de certains nutriments pour les régimes de 2000 et 2500 calories.
- Tenir des registres à l'appui de la déclaration de certains éléments nutritifs dans des circonstances précises
- Modifier la définition du récipient à usage unique
- Exiger un étiquetage en deux colonnes pour certains emballages
- Modifier les quantités de référence habituellement consommées qui sont utilisées par les fabricants pour déterminer la taille des portions sur l'étiquette
Afin de mieux comprendre à quoi ressemblera la nouvelle étiquette, la FDA fourni une comparaison côte à côte des anciennes et nouvelles étiquettes. Vous trouverez ci-dessous une adaptation de cette comparaison.
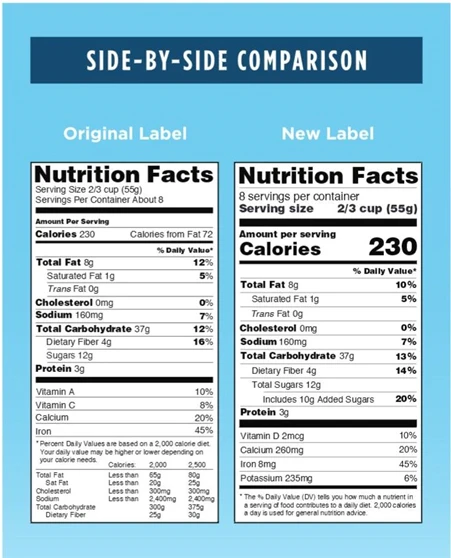
Alors que la date limite pour la mise en place de la réglementation finale sur l'étiquetage des nutraceutiques et des compléments alimentaires se rapproche, les fabricants et autres parties prenantes devraient planifier leur mise en conformité avec l'aide d'un expert en étiquetage spécialisé. Veillez à ce que l'étiquette de votre produit soit examinée dans les délais. Soyez informé. Soyez conforme.









