W regulacyjnym krajobrazie opieki zdrowotnej produkty skojarzone stanowią granicę innowacji, łącząc korzyści płynące z leków, urządzeń i leków biologicznych w jedno, potężne rozwiązanie terapeutyczne. Jednak z wielkimi innowacjami wiąże się wielka odpowiedzialność, szczególnie jeśli chodzi o zapewnienie bezpieczeństwa naszej najbardziej wrażliwej populacji - dzieci. Skupiając się na krytycznych imperatywach opakowań zabezpieczonych przed dziećmi, ten blog szczegółowo opisuje, w jaki sposób firmy z branży nauk przyrodniczych mogą poruszać się po tym złożonym terenie regulacyjnym.
Konwergencja technologii farmaceutycznych i urządzeń medycznych w produktach łączonych stawia wyjątkowe wyzwania w zakresie projektowania opakowań i zgodności z przepisami. Tradycyjne podejście do opakowań zabezpieczonych przed dziećmi może nie być wystarczające dla tych złożonych produktów, prowadząc do potencjalnych zagrożeń bezpieczeństwa i przeszkód regulacyjnych.
Niedawne wycofanie Produkty lecznicze znanych firm farmaceutycznych Produkty lecznicze z powodu nieodpowiednich opakowań zabezpieczających przed dostępem dzieci podkreśla znaczenie tej kwestii oraz potrzebę bardziej zróżnicowanego podejścia do bezpieczeństwa i zgodności z przepisami.
Uwagi do rozważenia:
- Zrozumienie ram regulacyjnych:
Produkty złożone podlegają jurysdykcji wielu organów regulacyjnych, przede wszystkim FDA Stanach Zjednoczonych. Główny sposób działania (PMOA) określa, które centrum w ramach FDA wiodącą rolę w zakresie regulacji – czy to Centrum Oceny i Badań Leków (CDER), Centrum Urządzeń i Zdrowia Radiologicznego (CDRH), czy Centrum Oceny i Badań Produktów Biologicznych (CBER). W przypadku opakowań zabezpieczonych przed dostępem dzieci najważniejsza jest zgodność z ustawą o opakowaniach zabezpieczających przed zatruciem (PPPA). - Rozważania projektowe:
Opracowanie opakowania zabezpieczającego przed dziećmi dla produktów łączonych wymaga delikatnej równowagi między bezpieczeństwem, użytecznością i funkcjonalnością. Innowacyjne projekty opakowań muszą nie tylko zapobiegać dostępowi dzieci, ale także zapewniać łatwość użytkowania dla dorosłych, zwłaszcza osób starszych lub niepełnosprawnych.
Często wymaga to nowatorskiego podejścia, takiego jak- Mechanizmy podwójnego działania (np. nasadki typu "naciśnij i przekręć")
- Technologie rozpraszania wzroku
- Systemy otwierania aktywowane wilgocią
- Perforowane blistry z określonymi wzorami rozdarć
- Testowanie i walidacja:
Rygorystyczne testy mają kluczowe znaczenie dla zapewnienia zgodności z normami dotyczącymi opakowań zabezpieczonych przed dziećmi. Zazwyczaj obejmuje to:- Testowanie protokołu z udziałem dzieci w wieku 42-51 miesięcy
- Testy przyjazne dla seniorów zapewniające dostępność dla dorosłych
- Testowanie stabilności w celu zapewnienia integralności opakowania przez cały cykl życia produktu.
- Zgłoszenia do organów regulacyjnych:
Przygotowanie kompleksowego wniosku regulacyjnego dla produktu złożonego z opakowaniem zabezpieczającym przed dziećmi obejmuje:- Szczegółowe specyfikacje opakowania i uzasadnienie projektu
- Wyniki testów odporności na dzieci i przyjazności dla osób starszych
- Dane dotyczące stabilności wykazujące skuteczność opakowania w czasie
- Analiza ryzyka i strategie jego ograniczania
Tabela: Kluczowe normy regulacyjne dotyczące opakowań zabezpieczających przed dziećmi w produktach łączonych
| Standard | Jurysdykcja | Koncentracja |
|---|---|---|
| 16 CFR 1700.20 | Stany Zjednoczone | Protokoły testowania opakowań wielokrotnego i jednorazowego użytku |
| ISO 8317 | Międzynarodowy | Wymagania dotyczące opakowań zabezpieczonych przed dziećmi z możliwością ponownego zamknięcia |
| EN 14375 | Europa | Opakowania jednorazowe dla produktów farmaceutycznych |
| BS EN 862:2005 | Europa | Opakowania jednorazowe dla produktów niefarmaceutycznych |
Rola partnerów regulacyjnych:
Poruszanie się po złożonym krajobrazie przepisów dotyczących produktów złożonych, zwłaszcza w odniesieniu do opakowań zabezpieczonych przed dziećmi, może być zniechęcające dla firm z branży nauk przyrodniczych. W tym przypadku kluczową rolę odgrywają partnerzy regulacyjni:
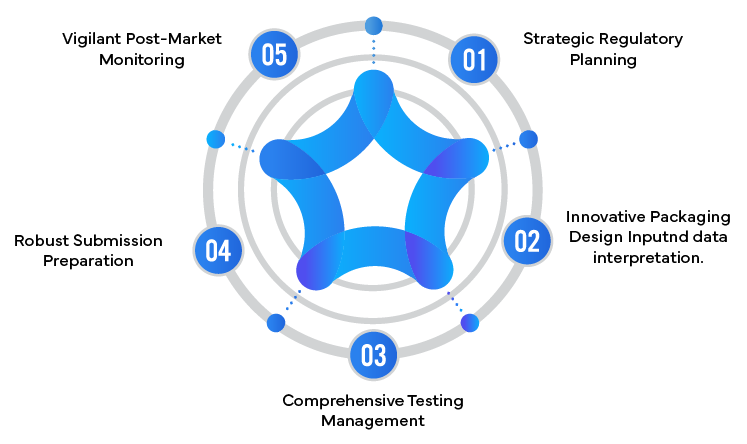
- Rozwój strategii regulacyjnej: Opracowanie kompleksowej strategii, która sprosta wyjątkowym wyzwaniom związanym z produktami łączonymi i wymogami dotyczącymi opakowań zabezpieczonych przed dziećmi.
- Wkład projektowy: Zapewnienie wglądu w projekt opakowania, który spełnia zarówno wymogi prawne, jak i potrzeby użytkowników.
- Koordynacja testów: Zarządzanie i interpretacja złożonych protokołów testowych w celu zapewnienia zgodności z normami dotyczącymi zabezpieczeń przed dziećmi.
- Przygotowanie wniosków: Opracowywanie solidnych wniosków do organów regulacyjnych, które skutecznie informują o bezpieczeństwie i skuteczności produktu.
- Nadzór po wprowadzeniu do obrotu: Wdrażanie systemów monitorowania działania i bezpieczeństwa produktów złożonych w rzeczywistych warunkach.
5 sposobów, w jakie partnerzy regulacyjni zwiększają bezpieczeństwo produktów łączonych
Podsumowanie:
Ponieważ produkty łączone nadal przesuwają granice innowacji medycznych, zapewnienie ich bezpieczeństwa poprzez skuteczne opakowanie zabezpieczające przed dziećmi pozostaje najważniejsze. Poruszanie się po złożonym krajobrazie regulacyjnym wymaga zniuansowanego zrozumienia zarówno przepisów farmaceutycznych, jak i przepisów dotyczących urządzeń medycznych, w połączeniu z innowacyjnym podejściem do projektowania opakowań.
Współpracując z doświadczonymi ekspertami ds. regulacji prawnych, firmy z branży nauk przyrodniczych mogą nie tylko zapewnić zgodność z przepisami, ale także wprowadzać innowacje w zakresie rozwiązań opakowaniowych, które chronią dzieci, jednocześnie zwiększając użyteczność dla wszystkich pacjentów. W tej ewoluującej dziedzinie kluczem do sukcesu jest zrównoważenie bezpieczeństwa, innowacyjności i znajomości przepisów - wyzwanie, które, jeśli zostanie podjęte, obiecuje odblokować nowe granice w opiece nad pacjentem i projektowaniu produktów.