En la industria farmacéutica, la seguridad de los pacientes y el cumplimiento normativo son fundamentales. Un aspecto crítico para garantizar ambos es la evaluación y el control de las impurezas genotóxicas en los medicamentos. La directriz M7 del Consejo Internacional de Armonización (ICH) proporciona un marco integral para gestionar estas impurezas, que pueden causar mutaciones genéticas y provocar cáncer. Las impurezas genotóxicas, incluso en cantidades mínimas, suponen un riesgo significativo para los pacientes. Estas impurezas pueden causar mutaciones genéticas, lo que podría provocar cáncer. Por lo tanto, la identificación adecuada, la evaluación de riesgos y el control de las impurezas genotóxicas son esenciales para mitigar estos riesgos y garantizar la seguridad y la eficacia de los productos farmacéuticos. Este blog explora los aspectos clave de ICH, los retos que aborda y el papel de los expertos en normativa para lograr el cumplimiento.
Aspectos clave de ICH
La directriz ICH describe un enfoque estructurado para la evaluación y el control de las impurezas genotóxicas. Abarca varios componentes clave:
Evaluación de riesgos
La evaluación del riesgo implica identificar las impurezas genotóxicas potenciales y evaluar su riesgo en función de su estructura química, los datos de compuestos similares y los datos toxicológicos disponibles. Este paso es crucial para determinar qué impurezas deben controlarse y a qué niveles.
Estrategias de control
Una vez identificadas las impurezas genotóxicas potenciales, deben aplicarse estrategias de control para limitar su presencia dentro de límites aceptables. Esto incluye el desarrollo y la validación de métodos analíticos para detectar impurezas y la aplicación de controles de fabricación para minimizar su formación.
Presentación reglamentaria
La documentación y justificación exhaustivas de las evaluaciones de riesgos y las estrategias de control son necesarias para la presentación de solicitudes a los organismos reguladores. Esto garantiza que los organismos reguladores dispongan de toda la información necesaria para evaluar la seguridad del medicamento.
Tabla 1: Componentes de ICH
| Componente ICH | Descripción |
|---|---|
| Evaluación de riesgos | Identifica y clasifica las impurezas en función de su potencial genotóxico. |
| Caracterización del riesgo | Evalúa los niveles de exposición y los riesgos potenciales para los pacientes |
| Medidas de control | Estrategias para limitar o eliminar las impurezas durante la producción |
(Sin limitarse a)
El papel de los expertos en regulación
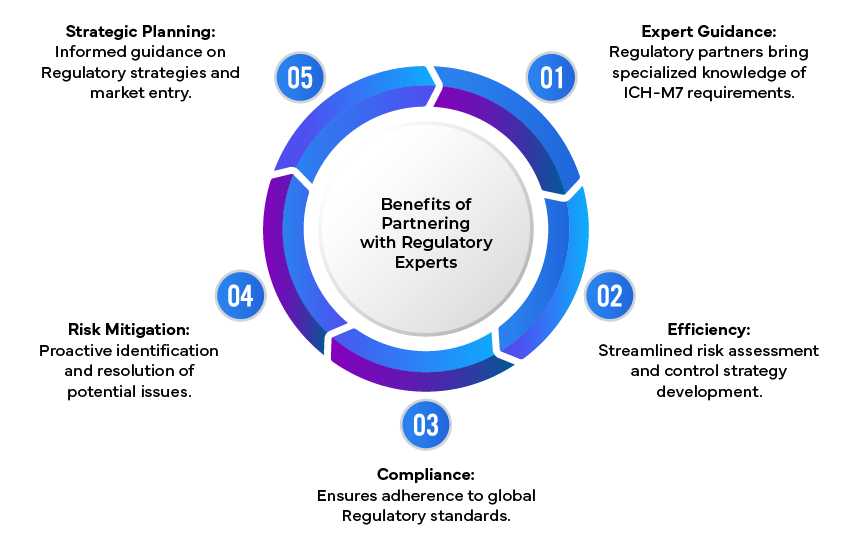
Navegar por los complejos requisitos ICH puede resultar complicado para las empresas farmacéuticas. Aquí es donde los expertos en regulación desempeñan un papel fundamental, al proporcionar orientación especializada sobre evaluaciones de riesgos, estrategias de control y la preparación de presentaciones reglamentarias exhaustivas. Al aprovechar su experiencia, las empresas pueden garantizar el cumplimiento de ICH y mitigar los posibles riesgos asociados a las impurezas genotóxicas.
Resumen
El cumplimiento de la directriz ICH es esencial para garantizar la seguridad y la eficacia de los productos farmacéuticos. Al adoptar un enfoque estructurado para la evaluación y el control de las impurezas genotóxicas, las empresas pueden proteger la seguridad de los pacientes y cumplir los requisitos reglamentarios. La colaboración con expertos en reglamentación agiliza aún más este proceso, ya que proporciona los conocimientos necesarios para navegar por los complejos entornos reglamentarios y lograr presentaciones satisfactorias.