
Récemment, l'apparition d'impuretés de nitrosamine dans certains médicaments génériques a entraîné une réévaluation des pratiques de l'industrie. Ce blog se penche sur les multiples facettes de l'atténuation des nitrosamines, en particulier dans le contexte des médicaments génériques. En outre, il met en lumière les considérations faites pour les impuretés liées à la substance médicamenteuse nitrosamine. Nous explorons les subtilités du maintien de la qualité, de l'assurance de la bioéquivalence et de la compréhension du rôle essentiel des experts en réglementation dans ce processus critique.
Le défi des nitrosamines : Un appel à l'action réglementaire
Les nitrosamines, une classe de composés connus pour être potentiellement cancérigènes, posent un défi réglementaire complexe. Les organismes de réglementation, notamment la FDA américaine FDA l'Agence européenne des médicaments (EMA), ont réagi en imposant des limites et des directives strictes concernant la présence de ces impuretés dans les produits pharmaceutiques. Cela nécessite une approche globale pour comprendre, détecter et atténuer le risque lié aux impuretés nitrosamines dans les médicaments génériques.
Les défis de la bioéquivalence dans les produits génériques : Équilibrer la sécurité et l'équivalence
La bioéquivalence est la pierre angulaire du développement des médicaments génériques, garantissant qu'un produit générique est thérapeutiquement équivalent à son homologue de référence. Cet aspect critique devient encore plus complexe dans le contexte de l'atténuation des impuretés liées aux nitrosamines.
1. Assurer la cohérence de la formulation
La présence d'impuretés de nitrosamine dépend de la délivrance cohérente de l'ingrédient pharmaceutique actif (IPA) au patient. Les experts en réglementation, en collaboration avec les scientifiques chargés de la formulation, jouent un rôle essentiel en veillant à ce que les ajustements effectués pour atténuer les impuretés ne compromettent pas la stabilité ou l'efficacité de la formulation.
2. Impacts sur l'absorption et la pharmacocinétique
Les impuretés de nitrosamine peuvent potentiellement affecter l'absorption et la pharmacocinétique du médicament. Ceci est particulièrement préoccupant dans le contexte des produits génériques, où des variations subtiles peuvent avoir des effets prononcés. Les experts en réglementation guident ces études pour s'assurer qu'elles respectent les normes réglementaires et fournissent des informations significatives sur la sécurité et l'efficacité du produit générique.
3. Études de dissolution : Un élément clé
Les impuretés de nitrosamine peuvent influencer les taux de dissolution, et les experts en réglementation travaillent en étroite collaboration avec les équipes de formulation et d'analyse pour développer et mettre en œuvre des méthodes robustes de test de dissolution. Ces méthodes doivent être suffisamment sensibles pour détecter les variations dans les profils de dissolution qui peuvent survenir en raison de la présence d'impuretés.
4. Suivi post-approbation et vigilance
Même après l'obtention de l'autorisation réglementaire, la surveillance des produits génériques pour détecter la présence d'impuretés nitrosamines se poursuit. Les études post-autorisation et les efforts de pharmacovigilance sont menés par des experts réglementaires qui travaillent en collaboration avec les fabricants pour mettre en œuvre des programmes de surveillance rigoureux. Cette vigilance constante est essentielle pour identifier et traiter rapidement tout problème de sécurité émergent lié aux impuretés nitrosamines.
Le rôle des experts en réglementation : Naviguer dans un paysage complexe
Les professionnels des affaires réglementaires jouent un rôle essentiel dans l'atténuation des problèmes posés par les impuretés liées aux nitrosamines dans les médicaments génériques. Leurs responsabilités multiples s'étendent à plusieurs domaines et sont illustrées dans le diagramme à secteurs ci-dessous :
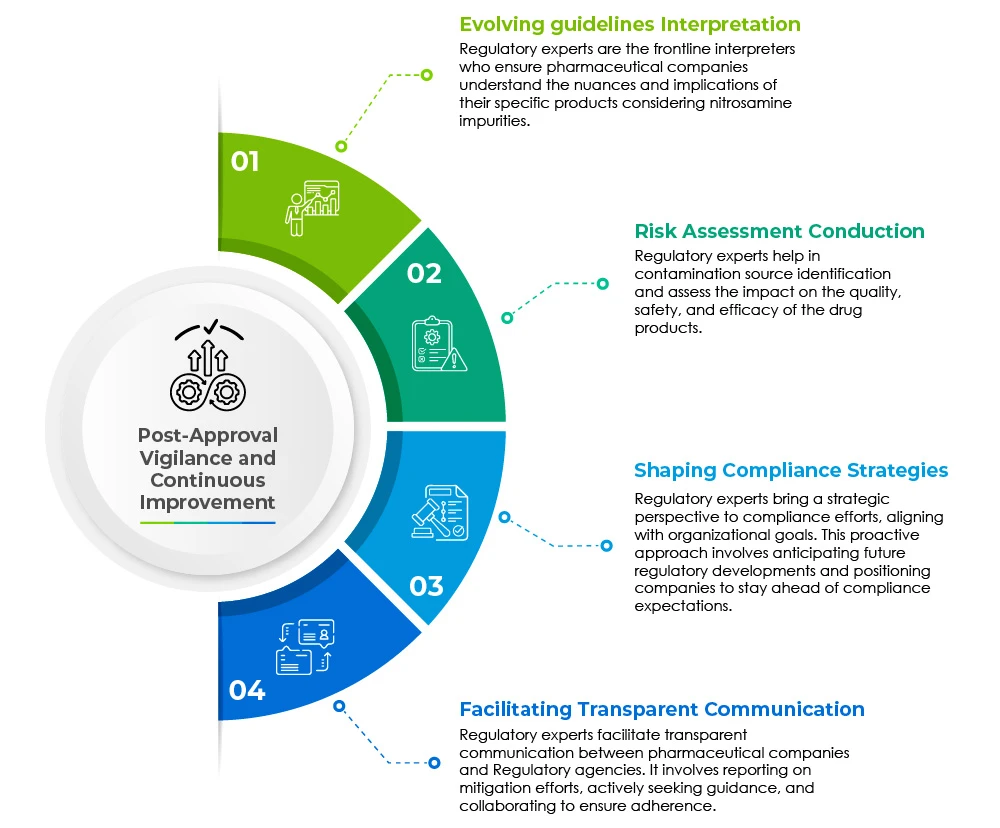
La vigilance post-approbation et l'amélioration continue sont les pierres angulaires d'une assistance réglementaire rapide.
Conclusion : Protéger la santé publique grâce à la vigilance et à l'expertise
La réduction des impuretés liées aux nitrosamines n'est pas seulement une exigence réglementaire, c'est aussi un engagement envers la santé publique. Alors que l'industrie pharmaceutique relève ce défi, le rôle des experts en réglementation devient primordial. Leur capacité à allier conformité et innovation garantit que les médicaments génériques non seulement répondent aux normes réglementaires, mais contribuent également à un avenir plus sûr et plus sain. Chez Freyr, nos experts en réglementation mettent à profit leur expertise pour obtenir un avantage concurrentiel dans ce domaine pour les entreprises pharmaceutiques. us pour en savoir plus.









