
Il est difficile pour les entreprises pharmaceutiques de connaître toutes les exigences réglementaires mondiales existantes en raison de l'évolution constante des réglementations et législations mondiales. De nouvelles procédures sont constamment développées et adoptées par les autorités réglementaires du monde entier en raison du processus d'harmonisation internationale.
HISTORIQUE DE L'INTELLIGENCE RÉGLEMENTAIRE (RI)
RI fait RI partie du département des affaires réglementaires mondiales d'une entreprise et élargit la fonction traditionnelle des affaires réglementaires au-delà de la préparation et de la soumission des demandes à la FDA aux agences réglementaires européennes et asiatiques.
Les dirigeants de l'entreprise sont tenus informés des réglementations en vigueur qui affectent le développement, l'approbation et l'entretien des produits, ainsi que de toute modification des réglementations et/ou du paysage réglementaire susceptible d'avoir une incidence sur leurs efforts.
RI aux résultats financiers de toutes les sociétés pharmaceutiques en aidant les équipes chargées des affaires réglementaires à fournir des dossiers de la plus haute qualité aux agences. Les entreprises doivent également comprendre les enjeux qui influent sur l'examen des demandes d'autorisation de mise sur le marché de nouveaux médicaments sur chaque marché mondial, au-delà des directives réglementaires.
L'ENVIRONNEMENT RÉGLEMENTAIRE
Les changements constants de l'environnement réglementaire obligent toutes les parties/autorités concernées à se tenir au courant des informations actuelles provenant de diverses sources. Les professionnels des affaires réglementaires peuvent s'appuyer sur les pratiques de l'industrie, les avis des agences de réglementation et les informations sur les concurrents pour élaborer des stratégies réglementaires fructueuses.
INTELLIGENCE RÉGLEMENTAIRE (RI)
RI à recueillir et à analyser des informations réglementaires afin d'évaluer l'impact ou les modifications apportées aux lois, réglementations, directives, documents d'orientation, etc. RI un professionnel de la réglementation de conseiller le personnel, RI répondre à des questions stratégiques en matière de réglementation et de rédiger ou d'élaborer une demande de commercialisation mondiale, ainsi que de déterminer les exigences relatives à la conduite d'essais cliniques mondiaux et à la fabrication.
RI des informations sur la recherche, le filtrage, l'analyse et l'application des informations afin de créer des renseignements réglementaires précieux. Les renseignements réglementaires suivent un processus systématique visant à rationaliser les fonctions au sein des affaires réglementaires.
COMMENT L'INTELLIGENCE RÉGLEMENTAIRE PEUT-ELLE VOUS AIDER ?
Avant de demander des autorisations cliniques, le service des affaires réglementaires pose quelques questions pour étudier les avantages et les inconvénients de l'introduction d'un médicament/produit particulier dans différentes régions et d'autres besoins en matière de conformité. Les questions de recherche sont déterminées par les besoins de l'entreprise et liées aux décisions et aux actions.
Le processus Regulatory Intelligence permet une analyse flexible des recherches. Il couvre de manière exhaustive toute la gamme de produits, notamment : les médicaments, les dispositifs médicaux, les produits biologiques, les produits vétérinaires, OTC grand public et OTC , ainsi que les nutraceutiques.
Les informations réglementaires comprennent : nouvelles directives, modification des directives, développement pharmaceutique, fabrication, qualité, clinique et non clinique, stabilité et stockage, validation, emballage et étiquetage, excipients pharmaceutiques, impuretés, Artwork matériel promotionnel, alerte de rappel,sécurité et pharmacovigilance, avertissements, formats de soumission et bien plus encore.
STRATÉGIE RÉGLEMENTAIRE MONDIALE : IMPORTANCE
Les changements dans le paysage mondial peuvent avoir une incidence sur la stratégie réglementaire mondiale, car de plus en plus d'entreprises mènent des essais et déposent des demandes de commercialisation dans le monde entier. RI comparent les évolutions réglementaires dans différents pays, évaluent l'adéquation des cadres réglementaires existants au regard des dernières avancées technologiques ou effectuent des analyses réglementaires dans le cadre de rapports de diligence raisonnable.
PRÉSÉANCE RÉGLEMENTAIRE
Une stratégie réglementaire peut être élaborée grâce à la surveillance et à la collecte d'RI peut aboutir à :
- Réduction du délai d'approbation
- Maximisation des marchés cibles
- Diminution du coût de développement des produits sur la base d'informations actualisées
SOURCES DE RENSEIGNEMENTS RÉGLEMENTAIRES
Prééminence réglementaire | Pratiques de l'industrie | Avis des agences réglementaires | Sites web des agences | Documents d'orientation | Courriers électroniques provenant des sites web réglementaires | Interactions avec les évaluateurs des agences | Lettres d'avertissement | Collègues et consultants | Demandes de liberté d'information| Informations sur les concurrents | Revues et bulletins d'information pertinents | Conférences pertinentes | Réunions consultatives | Interactions avec d'autres professionnels de la réglementation
LES ENTREPRISES PHARMACEUTIQUES ET L'INTELLIGENCE RÉGLEMENTAIRE
Les principales entreprises pharmaceutiques évaluent de nouveaux modèles commerciaux, notamment des plates-formes alternatives de gestion de l'information, afin de réduire les coûts, de raccourcir les délais et de maintenir la qualité et la conformité. Dans le contexte réglementaire actuel, la plupart des entreprises pharmaceutiques s'efforcent de maintenir la productivité de la recherche et du développement.
Les entreprises pharmaceutiques sont désireuses d'explorer de nouveaux modèles de développement de médicaments susceptibles de réduire les coûts de développement, d'accélérer les délais tout en maintenant la qualité et la conformité. Elles ont l'intention de réaliser ces gains en adoptant lentement de nouveaux modèles commerciaux pour la gestion des données et des réglementations.
Les sociétés pharmaceutiques étudient des plateformes de gestion de l'information innovantes capables de gérer l'ensemble des opérations liées aux données réglementaires et cliniques, avec un soutien dans toutes les zones géographiques et les agences de réglementation. Les plateformes de gestion de l'information rendent les données de recherche plus largement disponibles en normalisant la manière dont elles sont collectées, formatées et distribuées, et offrent des perspectives uniques au processus d'investigation.
Grâce aux outils et aux techniques d'analyse, les chercheurs peuvent modéliser les résultats, repérer les tendances et poser les bonnes questions, ce qui aidera les entreprises à normaliser et à optimiser leurs processus. Les efforts de réingénierie des processus impliqueront davantage d'activités dans les domaines de la réglementation, de la pharmacovigilance et des processus cliniques.
Celles-ci seront à leur tour aidées par une technologie intégrée et des capacités d'analyse permettant une conformité réglementaire globale. La modernisation rapide des opérations de développement vise en partie à éliminer les modèles de développement obsolètes, en particulier les solutions technologiques internes, ce qui permettra de compenser le ralentissement des taux de croissance et d'obtenir des résultats nets.
INTELLIGENCE ÉCONOMIQUE ET INDUSTRIE PHARMACEUTIQUE
Avec l'évolution des réglementations et des questions de conformité, les entreprises pharmaceutiques sont simultanément confrontées aux défis de la réduction des coûts, de l'augmentation des revenus et de l'efficacité opérationnelle, de la réduction des coûts de la chaîne d'approvisionnement, tout en répondant aux exigences réglementaires et de sécurité. Les entreprises pharmaceutiques peuvent utiliser stratégiquement des logiciels de veille stratégique pour prendre des décisions commerciales éclairées.
Le logiciel de veille stratégique peut analyser, rapporter et contrôler de grandes quantités de données grâce à l'architecture de veille stratégique et aider les entreprises à réduire leurs coûts, à augmenter leurs revenus et à maximiser la valeur de l'information.
RI POUR LES ENTREPRISES
Les grandes entreprises et les entreprises de taille moyenne dont les produits sont commercialisés sur de nombreux marchés sont confrontées à un véritable défi lorsqu'il s'agit d'obtenir des groupes de veille réglementaire des informations qui font autorité. Les entreprises supposent que les groupes de veille réglementaire fournissent une interprétation autorisée d'un large éventail de réglementations nationales et régionales. En outre, le groupe doit également fournir une évaluation de l'impact des changements réglementaires proposés sur de nombreux autres marchés.
RI : POINTS DOULEUREUX
Dans une enquête réalisée en 2014 sur RI centralisés RI , les personnes interrogées ont accordé une grande importance aux produits du RI , mais se sont déclarées peu satisfaites de ceux-ci.
• Le RI central est généralement situé au siège social de l'entreprise et est géré
par un personnel relativement restreint
• Le travail du RI central RI est souvent relativement vaste et associé à des missions critiques.
- Augmentation des exigences en matière d'information et d'audit par les autorités sanitaires
- 67% des entreprises ont mis en place un bureau/programme centralisé de veille réglementaire
• Un quart des répondants ont répondu « oui » à la question de savoir si le RI centralisé est considéré comme
la source qui fait autorité en matière de *services de renseignements matériels et immatériels
*Les services de renseignement durs et mous comprennent RI fondamentaux tels que l'interprétation des lois, les réglementations HA et les orientations.
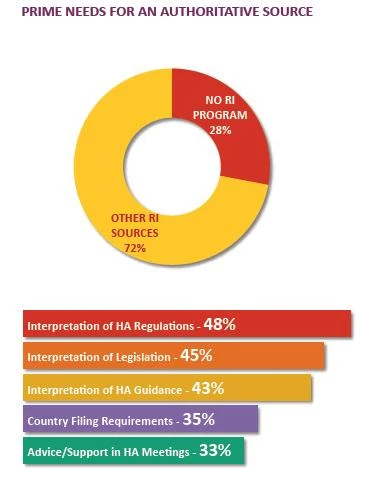
RAISONS POUR LESQUELLES LES PETITES ENTREPRISES DÉCLARENT RI COMME SOURCE FAIRE AUTORITÉ
- Faire appel à d'autres experts internes pour produire une analyse complète des règlements ou des orientations.
- Certaines parties prenantes s'appuient sur des réseaux internes et des sources externes pour élaborer un avis et un plan d'action afin de répondre aux nouvelles exigences réglementaires.
LES ENTREPRISES PRÉVOIENT UN CHANGEMENT DE
PROCESSUS : Améliorer la communication interne entre - le groupe central, les organismes de réglementation affiliés et les domaines fonctionnels
DES OUTILS DE GESTION DES PROCESSUS D'INFORMATION RÉGLEMENTAIRE : Améliorer l'accès à l'information grâce à des portails, des systèmes de gestion des connaissances et des outils externes.
RÔLES ET RESPONSABILITÉS : Changements organisationnels - Identifier et améliorer les prestations afin d'accroître la satisfaction des parties prenantes
INTELLIGENCE RÉGLEMENTAIRE AVANTAGES STRATÉGIQUES À LONG TERME
- Suivre l'environnement réglementaire et en assurer la conformité
- Gain de temps et d'argent grâce à la collecte, l'analyse et la diffusion de renseignements en temps réel
- Évite les risques de duplication et de redondance
- La barrière linguistique mondiale est surmontée grâce à l'accès instantané aux informations essentielles en anglais.
- Veiller à l'exactitude des informations critiques obtenues auprès des distributeurs, des fabricants et d'autres contacts industriels
- Entretenir la banque de données des connaissances en conservant et en enrichissant constamment les connaissances réglementaires
au sein de l'entreprise.
-Soutien à la création d'une politique réglementaire solide
- Examiner les anciennes données et contribuer à leur mise à jour en fonction des tendances réglementaires actuelles.
- Conseiller le personnel sur les nouvelles disciplines réglementaires en cours d'évolution
- Fournit des informations détaillées et personnalisées pour une recherche avancée
- Fournit un système de gestion de l'information centralisé et structuré
EN CONCLUSION
Toutes les entreprises pratiquent la veille réglementaire dans une certaine mesure et elles sont de plus en plus nombreuses à mettre en place des groupes de veille spécialisés. La portée de la veille réglementaire varie en fonction de la forme d'analyse et d'interprétation active, mais elle n'équivaut pas à l'information réglementaire.
En outre, il est impératif de disposer d'informations réglementaires, de répartir les tâches clés pour garantir la conformité, d'être conscient de l'avenir et de disposer de ressources adéquates. Le fait de disposer d'informations réglementaires correctes permet de concevoir et de mettre en œuvre une bonne stratégie réglementaire qui peut conduire à une réduction des délais de mise sur le marché grâce à un développement accéléré et à une évaluation de l'enregistrement plus aisée, à une réduction des coûts, à une conformité accrue et, en fin de compte, à l'optimisation du retour sur investissement.









