24 września 2016 r.; wraz z upływającym za miesiąc terminem zapewnienia zgodności urządzeń klasy II z unikalnym identyfikatorem urządzenia (UDI), zakładamy, jeśli nie na pewno, że wszyscy producenci urządzeń medycznych są dobrze wyposażeni w kompleksową mapę drogową regulacji. Oprócz solidnego opanowania wstępnych wymagań dotyczących zarządzania, oczekuje się, że producenci będą gotowi do audytu zgodności. Począwszy od walidacji rekordów identyfikatora urządzenia (DI) i identyfikatora produktu (PI) po udane zgłoszenia GUDID, powinni oni posiadać wiedzę na temat danych, które należy przedłożyć i procedur, których należy przestrzegać. Zarówno przed złożeniem wniosku, jak i po jego złożeniu, wyposażenie w lepszą wiedzę na temat know-how proceduralnego może uchronić producentów przed odpowiednimi wyzwaniami związanymi z agregacją danych, składaniem rekordów DI i zarządzaniem raportami dotyczącymi urządzeń, śledzeniem potwierdzeń HA itp.
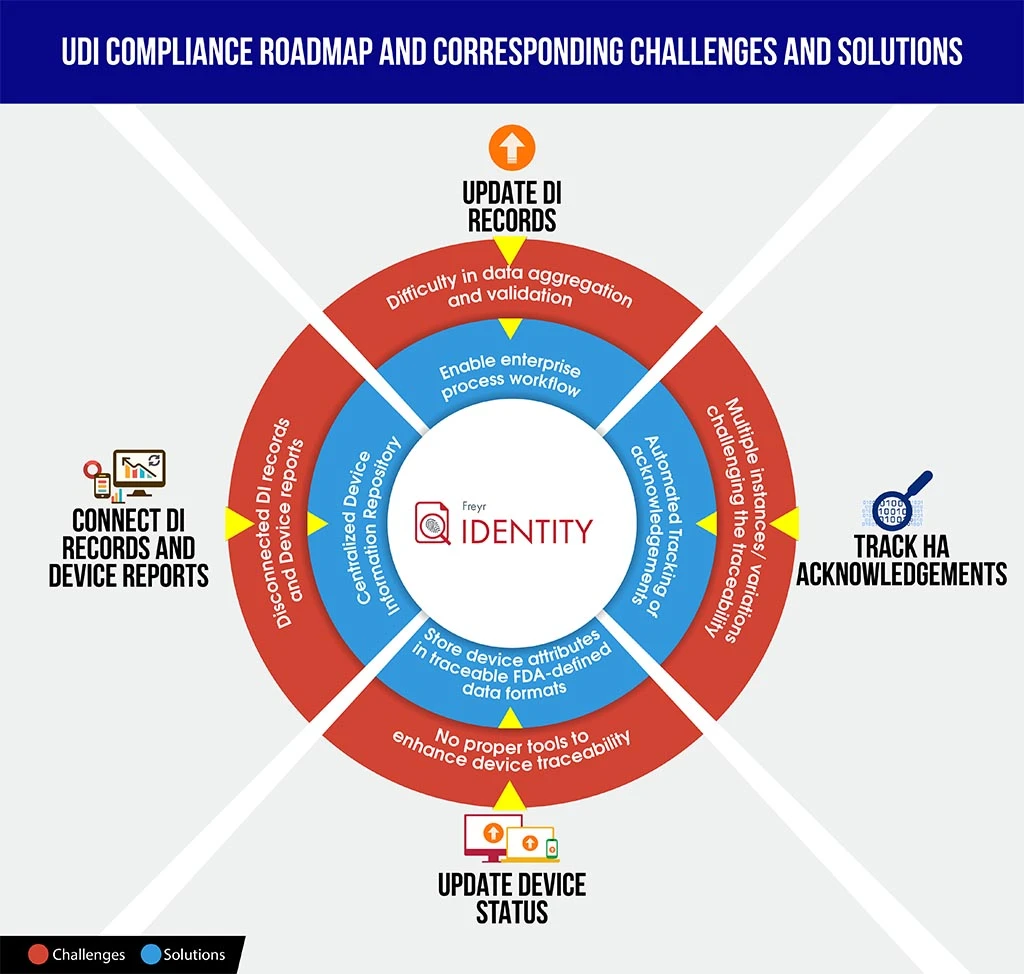
Aby wyposażyć producentów w lepszą pozycję w takich scenariuszach, przedstawiamy tutaj szybką do zrozumienia infografikę dotyczącą wyzwań związanych ze zgodnością z UDI i rozwiązań, która może zaoszczędzić czas na dekodowanie zawiłości związanych ze zgodnością oraz lepsze planowanie z wyprzedzeniem i strukturę mapy drogowej.
Aby pomóc Twojej organizacji sprawnie przejść przez ten złożony proces zapewnienia zgodności, Freyr najlepsze z obu światów – w pełni konfigurowalne oprogramowanie UDI dostępne na żądanie,Freyr , a także Centrum Doskonałości UDI (CoE), które oferuje najlepsze w swojej klasie, opłacalne i dostosowane do indywidualnych potrzeb usługi UDI, oparte na Twoich unikalnych i wymagających wymaganiach.









