
Zarządzanie ryzykiem jest krytycznym działaniem na wszystkich etapach cyklu życia urządzeń medycznych, ponieważ ma bezpośredni wpływ na bezpieczeństwo i dobre samopoczucie pacjentów. Ryzyko jest nieuniknione; można je jednak ograniczyć, jeśli firmy są świadome zbliżających się zagrożeń i przestrzegają skutecznych procedur zarządzania ryzykiem.
Failure Modes and Effects Analysis (FMEA) to narzędzie służące do identyfikacji możliwych awarii w projekcie, procesie produkcji lub montażu, produkcie lub usłudze w urządzeniu. "Tryby awarii" odnoszą się do sposobów, w jakie urządzenie może ulec awarii, co może potencjalnie wpłynąć na pacjentów. "Analiza skutków" odnosi się do badania konsekwencji tych awarii. Jest to podejście krok po kroku mające na celu zapewnienie niezawodności i jakości urządzenia.
Istnieją dwa rodzaje analiz FMEA: analiza FMEA projektu (DFMEA) oraz analiza FMEA procesu (PFMEA). W kontekście wyroby medyczne producenci urządzeń stosują analizę DFMEA do oceny awarii związanych z projektem i specyfikacjami urządzeń, natomiast analiza PFMEA służy do usprawniania procesu produkcji.
Chociaż FMEA obejmuje aspekt ryzyka, nie jest to system zarządzania ryzykiem. Wymagania dotyczące zarządzania ryzykiem zostały zdefiniowane w normie ISO 14971:2019, która służy jako ramy dla producentów wyrobów medycznych do przewidywania prawdopodobieństwa wystąpienia ryzyka i jego konsekwencji w całym cyklu życia produktu. Metodologia oceny ryzyka FMEA nie jest zgodna z normą ISO 14971:2019. FMEA ma własną międzynarodową normę IEC 60812:2018, która wyjaśnia, w jaki sposób planuje się, przeprowadza, dokumentuje i utrzymuje analizę trybów awarii i skutków. FMEA i ISO 14971 różnią się od siebie w pewnych aspektach, które są następujące:
Normalne użytkowanie i stan awarii
Zgodnie z normą ISO 14971 zarządzanie ryzykiem obejmuje zarówno normalne, jak i nieprawidłowe użycie urządzenia, podczas gdy FMEA obejmuje ryzyko związane wyłącznie z awarią urządzenia. Prostym przykładem może być ryzyko związane z linią dożylną (IV). Norma ISO 14971 uwzględnia potencjalne ryzyko infekcji pomimo prawidłowego podania kroplówki. Może to wynikać z różnych przyczyn, takich jak niska odporność pacjenta i infekcje występujące w szpitalu/środowisku klinicznym. Ryzyko to nie jest uwzględniane w ocenie FMEA. Chociaż producenci urządzeń medycznych nie mogą całkowicie uniknąć tego ryzyka, mogą uświadomić użytkownikom ryzyko szczątkowe związane z użytkowaniem urządzenia.
Ocena dotkliwości
ISO 14971 rozpatruje dotkliwość ryzyka w oparciu o szkody dla życia ludzi, podczas gdy FMEA rozpatruje to samo w oparciu o usterki w działaniu systemu. Stopień ryzyka może być uznany za niski w FMEA, jeśli wystąpi niewielka utrata funkcji, nawet jeśli może to doprowadzić do utraty życia. Ryzyko zostanie uznane za wysokie, jeśli urządzenie ulegnie awarii.
Na przykład FDA prowadnik (klasa I) przeznaczony do umieszczenia wewnątrz cewnika przezskórnego w celu skierowania cewnika przez naczynie krwionośne. Powłoka tego prowadnika może ulegać łuszczeniu. FMEA potencjalnie sklasyfikowała to jako przypadek o niskim ryzyku po ocenie, ale może to mieć poważne konsekwencje dla zdrowia pacjenta.
Procedura oceny ryzyka / trybów awarii
FMEA i ISO 14971 różnią się sposobem oceny ryzyka. W FMEA ryzyko jest oceniane poprzez identyfikację potencjalnych trybów i skutków awarii, a następnie uszeregowanie wagi awarii. Każda z potencjalnych przyczyn jest identyfikowana i określane jest prawdopodobieństwo jej wystąpienia. Ryzyko jest oceniane na podstawie numeru priorytetu ryzyka (RPN).
Mapowanie FMEA
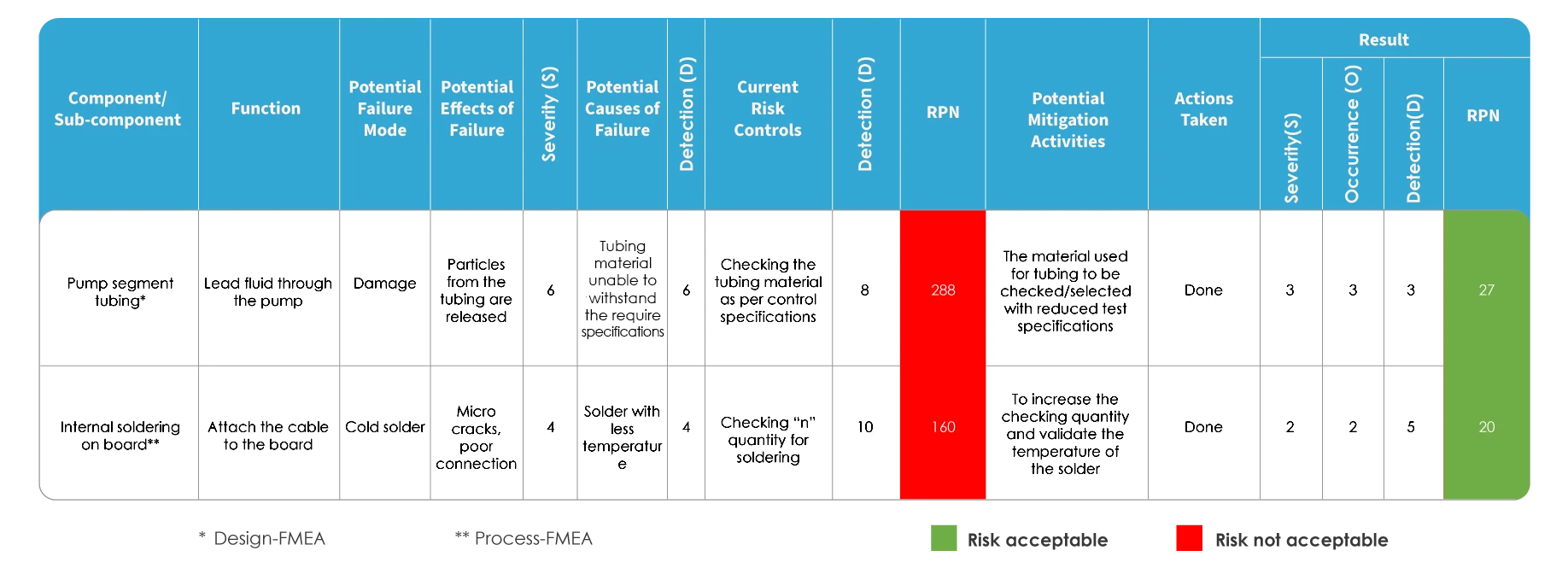
W przypadku mapowania zarządzania ryzykiem zgodnie z normą ISO 14971 stosuje się narzędzie identyfikowalności znane jako matryca identyfikowalności zagrożeń (Hazard Traceability Matrix, HTM). Obejmuje ono analizę ryzyka, ocenę, kontrolę i ocenę ryzyka rezydualnego.
Matryca identyfikowalności zagrożeń
| Analiza ryzyka | Ryzyko Eval. | Kontrola ryzyka | ||||||||||||
| ID | Zagrożenie | Racjonalnie przewidywalna sekwencja lub kombinacja zdarzeń | Niebezpieczne Sytuacja | Szkoda | Występowanie | Istotność | Dopuszczalne? | Opcje kontroli ryzyka i uzasadnienie | Kontrola ryzyka Środki | Ryzyko Kontrola Weryfikacja | Status | Potencjał ryzyka | Poziom ryzyka | Ryzyko rezydualne |
| 1 | Napięcie sieciowe | Użytkownik korzysta z urządzenia | Użytkownik/pacjent może być narażony na działanie napięcia sieciowego podczas kontaktu z urządzeniem. | Śmierć użytkownika/pacjenta | 5 | 5 | N | Bezpieczeństwo dzięki zmianie projektu i wprowadzeniu środków ochronnych. | Konstrukcja zgodna z normą IEC 61010. | Testy elektryczne należy przeprowadzać zgodnie z normą IEC 61010 | Gotowe | 2 | 2 | Y |
![]()
Po omówieniu różnic między nimi można stwierdzić, że ISO 14971 stosuje kompleksowe podejście do zarządzania ryzykiem, podczas gdy FMEA jest bardziej narzędziem niezawodności. Niemniej jednak, producenci urządzeń medycznych musieliby stosować się do normy ISO 14971, aby spełnić oczekiwania organów regulacyjnych w zakresie standardów zarządzania ryzykiem.
Aby dowiedzieć się więcej na temat zgodności z normą ISO 14971:2016 i usług doradczych w zakresie zarządzania ryzykiem, skontaktuj się Freyr już dziś!









