
En el panorama altamente regulado de la industria de las ciencias de la vida, el cumplimiento de las directrices específicas del producto (PSG) es fundamental para el éxito del desarrollo y la aprobación de fármacos. Se trata de documentos exhaustivos emitidos por las autoridades sanitarias mundiales para orientar sobre la aprobación de productos farmacéuticos dentro de categorías terapéuticas específicas.
Este blog detalla el propósito, la relevancia y la perspectiva de la HA sobre la emisión de las PSG. En este artefacto se detallan la justificación y las expectativas establecidas en las PSG que permiten el éxito estratégico de las empresas de ciencias de la vida.
Entender las directrices específicas de cada producto y sus tipos
Los PSG desempeñan un papel fundamental en la configuración de la vía reguladora de los productos farmacéuticos. Al proporcionar orientaciones específicas, los PSG garantizan la coherencia y la solidez de las evaluaciones de las solicitudes de productos dentro de categorías terapéuticas concretas. Al adherirse a los PSG, las empresas farmacéuticas pueden navegar por el intrincado panorama regulador, garantizando que sus productos cumplen las normas de seguridad y eficacia requeridas.
Los PSG no se limitan al desarrollo de medicamentos genéricos. También abarcan una amplia gama de productos farmacéuticos, como los siguientes:
- Para medicamentos innovadores: Las PSG ofrecen orientación específica sobre estudios preclínicos, diseño de ensayos clínicos, evaluación de la seguridad, farmacocinética y criterios de valoración de la eficacia. Orientan a las empresas sobre el tipo y la cantidad de datos necesarios para demostrar la seguridad y eficacia de sus medicamentos innovadores.
- Para biosimilares: Las PSG describen los requisitos de datos, métodos analíticos y consideraciones de diseño de estudios clínicos para productos biosimilares. Al seguirlas, las empresas de biosimilares pueden demostrar la similitud de sus productos con el biológico de referencia, allanando el camino para la aprobación y el acceso al mercado.
- Para los productos biológicos: Estas directrices abordan aspectos críticos, como la fabricación, la caracterización y los estudios de comparabilidad, garantizando que los productos biológicos cumplen las normas aprobadas.
Desarrollo de directrices y procesos específicos para cada producto
El desarrollo de los PSG es un esfuerzo de colaboración en el que participan las autoridades sanitarias, los expertos científicos y las partes interesadas del sector. A continuación se exponen las fases de desarrollo de las PSG:
Etapa 1 - Evaluación exhaustiva del área terapéutica: Las autoridades sanitarias identifican las lagunas en las directrices existentes e inician la elaboración de directrices para abordarlas. A continuación, los expertos científicos y las partes interesadas de la industria contribuyen con su experiencia para garantizar que el borrador de las directrices esté basado en pruebas y sea práctico de aplicar.
Fase 2 - Consulta pública: Los borradores de las directrices están ahora a disposición del público para su revisión y comentarios. Este enfoque abierto y transparente permite a las partes interesadas, incluidos los profesionales de la salud (HCP), grupos de pacientes y representantes de la industria, para proporcionar información valiosa y mejorar la calidad general y la pertinencia de las directrices.
Fase 3Etapa de revisión interna: Mientras los borradores de las directrices se someten a consulta pública, el equipo de desarrollo de las directrices dentro de las autoridades sanitarias lleva a cabo una rigurosa revisión interna, asegurándose de que las directrices cumplen los requisitos normativos necesarios y se ajustan al marco normativo general.
Fase 4 - Finalización: Una vez finalizadas, las GSP se publican y se ponen a disposición del sector, proporcionando orientaciones claras y prácticas para el desarrollo y la presentación de productos.
Componentes de los PSG
Las empresas de ciencias de la vida deben comprender claramente los componentes de los PSG. El siguiente gráfico circular los ilustra en detalle:
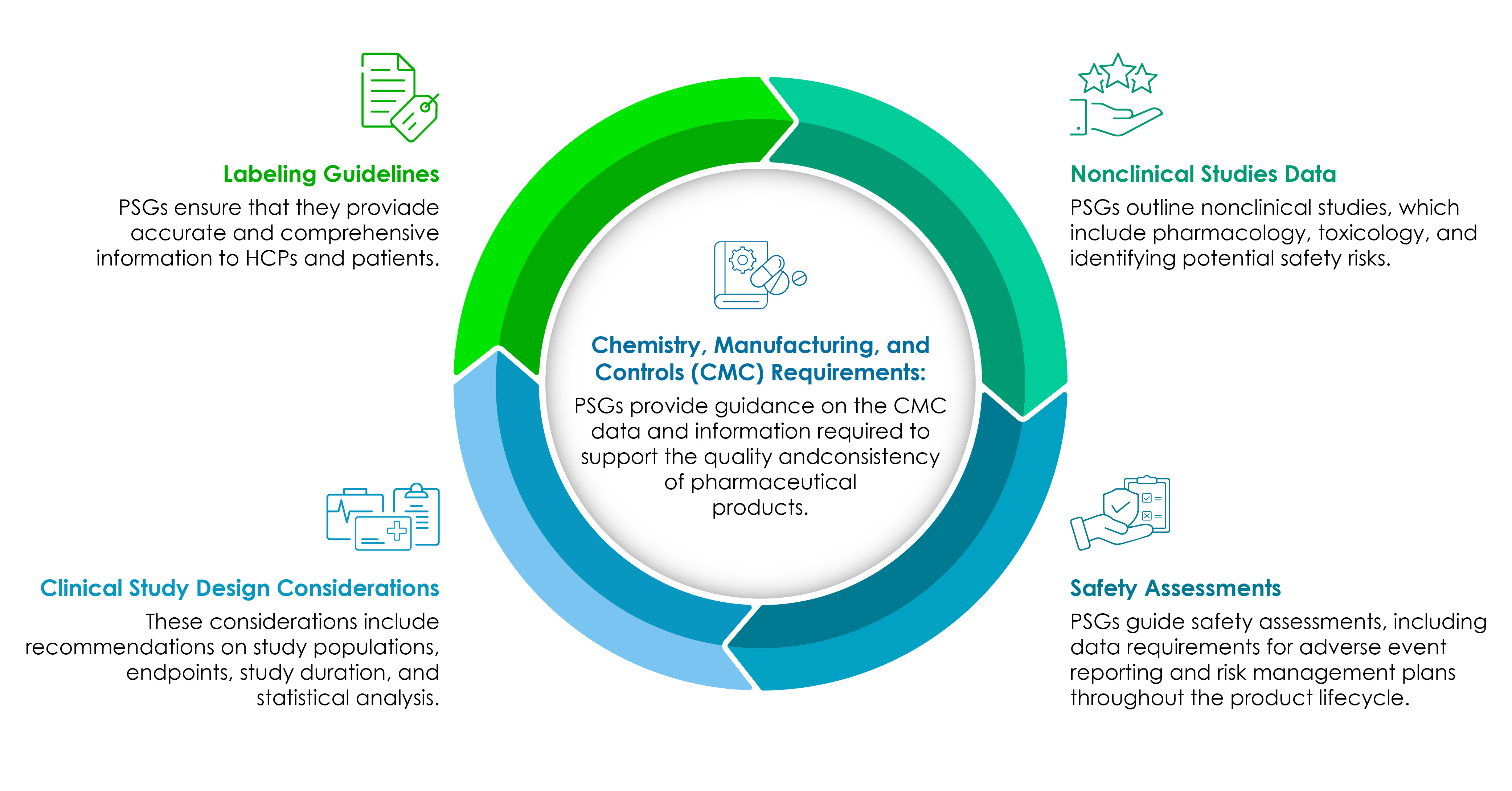
CMC el núcleo de todo desarrollo de productos farmacéuticos centrado en la normativa.
Navegar por los PSG
La navegación por los PSG de conformidad con la normativa puede lograrse mediante los siguientes puntos/estrategias:
- Compromiso temprano con las autoridades sanitarias: Este compromiso fomenta la colaboración y ayuda a abordar posibles problemas de forma proactiva.
- Experiencia científica: Las aportaciones de expertos garantizan que los diseños de los estudios, los métodos analíticos y las evaluaciones de seguridad se ajusten a las normas científicas más exigentes.
- Consultores reguladores: Los consultores proporcionan orientación experta, garantizando el éxito de los planes de desarrollo y las presentaciones reglamentarias.
- Revisión exhaustiva de las PSG: Las empresas deben identificar las secciones específicas de PSG aplicables a su producto y alinear sus planes de desarrollo en consecuencia.
- Seguimiento continuo: Las PSG son documentos dinámicos que pueden sufrir actualizaciones o revisiones con frecuencia. Las empresas deben supervisar los cambios en las PSG para garantizar el cumplimiento normativo de los requisitos más recientes de las PSG.
La orientación normativa de expertos facilita la navegación por la PSG. Consulte ahora
Conclusión
Las directrices específicas de producto (PSG) constituyen la espina dorsal de las presentaciones reglamentarias para productos farmacéuticos dentro de categorías terapéuticas específicas. Para las empresas de ciencias de la vida que desean agilizar las aprobaciones, garantizar la calidad de los productos y navegar sin problemas por el panorama normativo mundial, es fundamental comprender las perspectivas de la Autoridad Sanitaria que subyacen a la emisión de las directrices.
Como proveedor líder de servicios normativos, Freyr la importancia de adherirse a las mejores prácticas y aprovechar la experiencia que guiará a las empresas de ciencias de la vida a alinear sus estrategias de desarrollo de productos con los requisitos del PSG. us hoy mismo para obtener más información sobre nuestros servicios y cómo podemos ayudarle a alcanzar sus objetivos.









