
En los últimos tiempos, la aparición de impurezas de nitrosamina en determinadas sustancias de medicamentos genéricos ha provocado una reevaluación de las prácticas de la industria. Este blog profundiza en el polifacético mundo de la mitigación de las nitrosaminas, concretamente en el contexto de los medicamentos genéricos. Además, también arroja luz sobre las consideraciones realizadas para las impurezas relacionadas con las sustancias farmacológicas nitrosamínicas. Exploramos las complejidades de mantener la calidad, garantizar la bioequivalencia y comprender el papel fundamental de los expertos reguladores en este proceso crítico.
El reto de las nitrosaminas: Una llamada a la acción reguladora
Las nitrosaminas, una clase de compuestos conocidos por ser potenciales carcinógenos, plantean un complejo desafío normativo. Las agencias reguladoras, entre ellas la FDA de EE. UU. FDA la Agencia Europea de Medicamentos (EMA), han respondido con límites y directrices estrictos para la presencia de estas impurezas en los productos farmacéuticos. Esto requiere un enfoque integral para comprender, detectar y mitigar el riesgo de las impurezas de nitrosamina en los medicamentos genéricos.
Retos de bioequivalencia en los productos genéricos: Equilibrio entre seguridad y equivalencia
La bioequivalencia es la piedra angular del desarrollo de medicamentos genéricos, ya que garantiza que un producto genérico sea terapéuticamente equivalente a su homólogo de referencia. Este aspecto crítico se vuelve aún más intrincado en el contexto de la mitigación de las impurezas relacionadas con las nitrosaminas.
1. Garantizar la coherencia en la formulación
La presencia de impurezas de nitrosamina condiciona el suministro constante del principio activo farmacéutico (API) al paciente. Los expertos en reglamentación, en colaboración con los científicos de formulación, desempeñan un papel fundamental a la hora de garantizar que los ajustes realizados para mitigar las impurezas no comprometan la estabilidad o la eficacia de la formulación.
2. Efectos sobre la absorción y la farmacocinética
Las impurezas de nitrosamina pueden afectar potencialmente a la absorción y farmacocinética del medicamento. Esto es especialmente preocupante en el contexto de los productos genéricos, en los que variaciones sutiles pueden tener efectos pronunciados. Los expertos en reglamentación guían estos estudios para garantizar que cumplen las normas reglamentarias y proporcionan información significativa sobre la seguridad y eficacia del producto genérico.
3. Estudios de disolución: Un componente clave
Las impurezas de las nitrosaminas pueden influir en las velocidades de disolución, por lo que los expertos en reglamentación colaboran estrechamente con los equipos de formulación y análisis para desarrollar y aplicar métodos sólidos de ensayo de disolución. Estos métodos deben ser lo suficientemente sensibles como para detectar variaciones en los perfiles de disolución que puedan surgir debido a la presencia de impurezas.
4. Seguimiento y vigilancia tras la aprobación
Incluso después de la aprobación reglamentaria, continúa la supervisión de los productos genéricos para detectar la presencia de impurezas de nitrosamina. Los estudios posteriores a la aprobación y las iniciativas de farmacovigilancia están dirigidos por expertos en reglamentación que colaboran con los fabricantes para implementar programas de supervisión sólidos. Esta vigilancia continua es fundamental para identificar y abordar rápidamente cualquier problema de seguridad emergente relacionado con las impurezas de nitrosamina.
El papel de los expertos en regulación: Navegar por el complejo panorama
Asuntos Regulatorios desempeñan un papel fundamental en la mitigación de los retos que plantean las impurezas relacionadas con las nitrosaminas en los medicamentos genéricos. Sus responsabilidades multifacéticas se extienden a diversos ámbitos y se recogen en el siguiente gráfico circular:
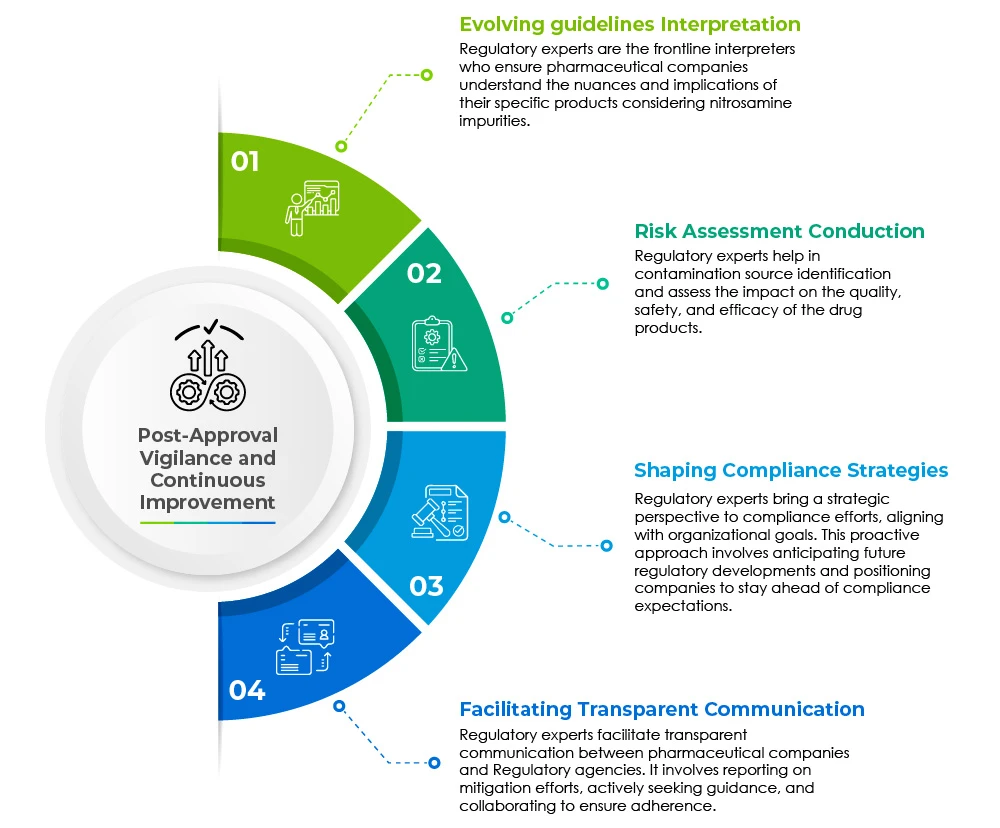
La vigilancia posterior a la homologación y la mejora continua son las piedras angulares de una asistencia reglamentaria rápida.
Conclusiones: Salvaguardar la salud pública mediante la vigilancia y la experiencia
Mitigar las impurezas relacionadas con las nitrosaminas no es solo un requisito normativo, sino un compromiso con la salud pública. A medida que la industria farmacéutica afronta este reto, el papel de los expertos en normativa cobra una importancia fundamental. Su capacidad para combinar el cumplimiento normativo con la innovación garantiza que los medicamentos genéricos no solo cumplan las normas reglamentarias, sino que también contribuyan a un futuro más seguro y saludable. En Freyr, nuestros expertos en normativa aprovechan sus conocimientos para obtener una ventaja competitiva en este ámbito para las empresas farmacéuticas. us para obtener más información.









