Serviços de regulamentação de dispositivos médicos
em Singapura Visão geral
Os dispositivos médicos em Singapura são regulamentados pela Lei dos Produtos de Saúde (HPA) e pelos seus Regulamentos relativos aos Produtos de Saúde (Dispositivos Médicos) de 2010.
Autoridade reguladora: Autoridade para as Ciências da SaúdeHSA)
Regulamento: Regulamentos relativos aos produtos de saúde (dispositivos médicos) de 2010
Via de regulação: Secção de Dispositivos Médicos da Autoridade para as Ciências da SaúdeHSA)
Representante autorizado: Singapura Registado
Requisito do SGQ: SS 620:2016, Norma de Singapura para Boas Práticas de Distribuição de Dispositivos Médicos, e ISO 13485:2016
Avaliação dos dados técnicos: Autoridade para as Ciências da SaúdeHSA)
Validade da licença: Todas as licenças de concessionário são válidas por 12 meses a partir da data de aprovação
Labelling : Orientações regulamentares, GN- 23 Revisto (1 de março de 2020)
Formato de apresentação: Online
Língua: Inglês
Classificação de dispositivos médicos HSA
HSA aplica 16 conjuntos de regras para classificar os dispositivos médicos, do risco mais baixo ao mais elevado, nas classes A, B, C e D.
A classificação do risco depende de factores como a duração do contacto, o grau de invasividade, a utilização prevista e o método de administração.
Classificação dos dispositivos médicos, HSA
| Classe de risco | Nível de risco | Exemplos de dispositivos médicos |
|---|---|---|
| Classe A | Baixo risco | Visor de filmes, mão cirúrgica, bainha, máscara de oxigénio |
| Classe B | Risco baixo a moderado | Manguito de pressão arterial, esterilizador de haste |
| Classe C | Risco moderado a elevado | Monitor do paciente, mesin X-ray |
| Classe D | Risco elevado | Stents cardíacos, pacemakers |
Classificação IVD
Os dispositivos médicos in vitro são classificados a seguir, do risco mais baixo ao mais elevado.
Classe de risco | Nível de risco | Exemplos de dispositivos médicos in vitro |
|---|---|---|
| Classe A | Baixo risco individual e baixo risco para a saúde pública | Recetáculo de amostras |
| Classe B | Risco individual moderado ou risco baixo para a saúde pública ou ambos | Vitamina B12, auto-diagnóstico de gravidez, anticorpo anti-nuclear, tiras de teste de urina |
| Classe C | Risco individual elevado ou risco moderado para a saúde pública ou ambos | Auto-diagnóstico da glucose no sangue, tipagem HLA, rastreio PSA , Rubéola IgM |
| Classe D | Elevado risco individual e elevado risco para a saúde pública | Rastreio do VIH em dadores de sangue, kit de diagnóstico do VIH |
Singapore Medical Device Authorized Representative / Registrant
Um Registrante é o elo de ligação entre a sua empresa e HSA, que trata do registo de dispositivos em Singapura. O representante autorizado de dispositivos médicos de Singapura processa o submissão da HSA é responsável pelo registo HSA seu HSA . Apenas empresas ou entidades sediadas em Singapura podem atuar como Registrantes; estas também devem estar registadas na HSA.
Registo de Dispositivos Médicos HSA
O processo de registo de dispositivos HSA é realizado através do sistemaonline de Informação e Comunicação sobre Dispositivosonline (MEDICS) HSA . Cada registo HSA é feito através de uma via de avaliação específica, dependendo do seguinte:
- Classificação de risco do dispositivo.
- Número de aprovações prévias concedidas pelas agências reguladoras de referência no estrangeiro.
- Duração do historial de comercialização de segurança do dispositivo.
A rota de avaliação do dispositivo determinará o tempo de resposta (TAT), as taxas e os documentos necessários para o registo.
Registo Classe A - Os dispositivos médicos Classe A estão isentos do registo do produto. No entanto, é necessário preencher a lista de isenção Classe A no MEDICS durante a submissão da licença do distribuidor.
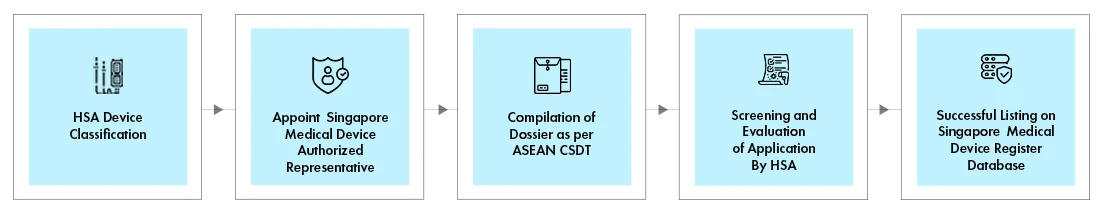
Fluxo do processo
Gestão do ciclo de vida do dispositivo pós-aprovação
Freyr fabricantes estrangeiros na gestão end-to-end do ciclo de vida dos dispositivos end-to-end , incluindo atividades pós-aprovação, tais como:
- Gestão de alterações pós-aprovação - alterações às aprovações de dispositivos médicos existentes, tais como a adição de novas variantes e acessórios; a adição de novas indicações de utilização, entre outras.
- Manutenção das aprovações e registos dos dispositivos médicos através do pagamento atempado das taxas administrativas e de registo.
- Renovação da licença.
Com uma equipa profissional para fornecer apoio regulamentar, Freyr apoia os fabricantes na manutenção da qualidade e segurança necessárias para a aprovação. Os especialistas em inteligência da Freyrobservam atentamente as actualizações regulamentares e informam os clientes sobre as medidas a tomar para que o produto esteja em conformidade com as normas em vigor.
Resumo
O tempo de processamento para o registo de produtos é mencionado no quadro seguinte.
| Classe de risco | Imediato | Expedito | Abreviado | Avaliação completa | Total (regime de revisão prioritária) |
|---|---|---|---|---|---|
| Classe B | Registo imediato após a apresentação | 100 dias úteis | 160 dias úteis | 120 dias úteis | |
| Classe C | Registo imediato após o envio ( submissão para submissão médica móvel autónoma de Classe C) | 120 dias úteis | 160 dias úteis | 220 dias úteis | 165 dias úteis |
| Classe D | 180 dias úteis | 220 dias úteis | 310 dias úteis | 235 dias úteis | |
| Classe D (dispositivos que incorporam Medicamentos) | 220 dias úteis | 310 dias úteis |
O prazo de entrega para uma alteração de registante é de 40 dias úteis.
NOTA-
- Os dispositivos médicos da classe A estão isentos de registo de produtos.
- O tempo de execução exclui o tempo necessário para responder a quaisquer pedidos de esclarecimento ou de informações adicionais por parte da HSA durante a fase de avaliação.
Especialização em Freyr
- Diligência devida regulamentar para o registo de dispositivos na HSA, Singapura
- Classificação e agrupamento de dispositivos médicos HSA
- Apoio à avaliação do Organismo de Avaliação da Conformidade (OAC)
- Modelo de Dossiê Comum da ASEAN (CSDT) Compilação do Dossiê
- Registo de dispositivos HSA ;
- Representação legal
- Apoio à rotulagem
- Identificação e qualificação de distribuidores
- Vigilância Pós-Comercialização
- Gestão de alterações pós-aprovação
- Renovação e transferência de licenças
- Serviços de apresentação e de ligação com a HSA