No cenário em constante evolução do desenvolvimento farmacêutico, o caminho desde a descoberta em laboratório até ao tratamento do paciente é pavimentado com desafios regulatórios complexos. Neste processo encontra-se a submissão de novos medicamentos submissão NDA), um marco crítico que engloba esforço científico e investimento. Este blogue aprofunda as complexidades das operações NDA , oferecendo insights valiosos e lições aprendidas com veteranos da indústria.
NDA
Os pedidos de registro de novos medicamentos representam o culminar de extensa pesquisa, desenvolvimento e testes clínicos. Eles servem como um dossiê abrangente que convence as autoridades regulatórias, como a Food and Drug Administration (FDA) dos EUA, de que um novo medicamento é seguro, eficaz e está pronto para aprovação no mercado.
A complexidade do NDA de NDA
Um dos principais obstáculos nas NDA é o grande volume e a complexidade dos dados exigidos. As empresas farmacêuticas precisam navegar por um labirinto de diretrizes regulatórias enquanto apresentam evidências claras e convincentes dos méritos dos seus produtos farmacêuticos. Esse equilíbrio muitas vezes leva a atrasos, revisões dispendiosas e, em alguns casos, rejeições definitivas.
Para esclarecer este processo crítico, vamos analisar as principais etapas da NDA e explorar estratégias para o sucesso em cada etapa.
Tabela 1: Principais etapas na NDA
| Estágio | Descrição | Melhores práticas |
|---|---|---|
| Investigação pré-clínica | Estudos em laboratório e em animais para recolha de dados iniciais | Assegurar uma conceção sólida do estudo e uma recolha meticulosa de dados |
| Ensaios clínicos | Ensaios em humanos efectuados em fases (I, II, III) | Implementar protocolos rigorosos e manter a integridade dos dados |
| Documentação | Compilação de dados de segurança, eficácia e qualidade | Organizar os dados de forma sistemática e garantir a clareza da apresentação |
| Revisão regulamentar | Submissão à FDA processo de revisão | Manter uma comunicação aberta com os organismos reguladores |
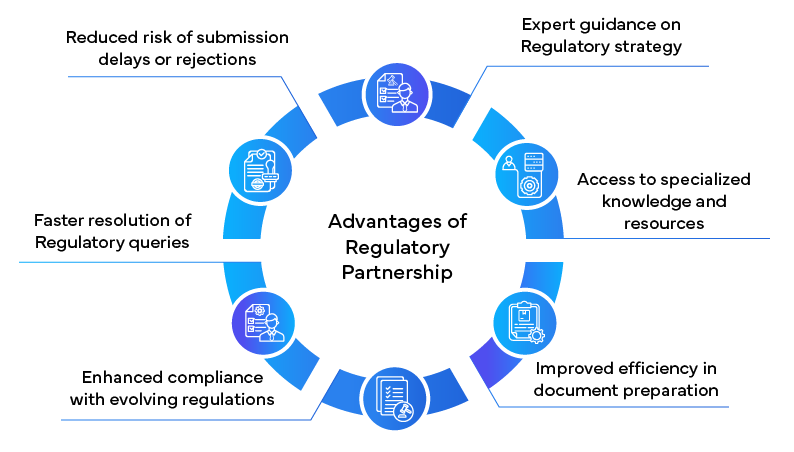
Papel da parceria de regulamentação
Ao navegar pelo complexo NDA , muitas empresas farmacêuticas estão a recorrer a parceiros regulatórios para obter apoio. Essas empresas especializadas oferecem uma vasta experiência e conhecimento que podem simplificar significativamente o NDA .
Lições aprendidas
À medida que olhamos para o futuro, a importância de operações NDA eficazes NDA só tenderá a crescer. Com o ritmo da inovação a acelerar e o panorama regulatório em evolução, aqueles que dominarem esse processo crítico estarão em melhor posição para levar tratamentos transformadores a pacientes em todo o mundo.
O caminho para uma NDA bem-sucedida NDA raramente é simples. Além disso, ao adotar uma abordagem estratégica para as operações regulatórias, aproveitar parcerias com especialistas e manter um compromisso com a qualidade e a conformidade, as empresas farmacêuticas podem melhorar significativamente as suas chances de NDA .