
A publicidade farmacêutica, incluindo a publicidade direta ao consumidor, é regulamentada pelo Gabinete de Promoção de Medicamentos Sujeitos a Receita Médica (OPDP) da Administração de Alimentos e Medicamentos dos Estados Unidos (US FDA), pelo Departamento de Publicidade e Rotulagem Promocional (APLB) do Centro de Avaliação e Investigação de Medicamentos (CDER) e pelo Centro de Avaliação e Investigação Biológica (CBER), respetivamente. As informações enviadas ao OPDP e ao APLB ser precisas, éticas e não enganosas. Informações adicionais sobre os benefícios e riscos do produto devem ser incluídas no envio. Os escritórios também analisam os materiais promocionais enviados à agência.
Em abril de 2022, aFDA US FDA orientações sobre os envios de material promocional de rotulagem e publicidade. As orientações ajudam a compreender o envio eletrónico no Módulo 1 do eCTD, utilizando a versão 3.3 ou superior do ficheiro US. O documento inclui uma menção aos tipos de materiais promocionais não sujeitos ao envio eletrónico obrigatório nos termos da secção 745A. As cópias em papel de todos os tipos de envios promocionais serão aceites até vinte e quatro (24) meses após publication das orientações.
Exceção
O documento afirma que os envios nos termos da secção 505(b), (i) ou (j) da Lei Federal sobre Alimentos, Medicamentos e Cosméticos (FD&C Act) e os envios nos termos da secção 47 351(a) ou (k) da Lei dos Serviços de Saúde Pública (PHS Act) devem ser apresentados em formato eletrónico, conforme definido pela FDA. Este documento não está sujeito às restrições habituais dos regulamentos de boas práticas de orientação FDA, uma vez que não está legalmente estabelecido para responsabilidades executórias. Portanto, a parte desta orientação que estabelece a exigência de submissões eletrónicas nos termos da secção 745A(a) da FD&C Act tem efeito vinculativo, conforme indicado pelo uso das palavras deve, terá ou exigido.
A FDA o material promocional redigido no prazo de quarenta e cinco (45) dias após a apresentação voluntária pelos patrocinadores. Para quaisquer questões relacionadas com o produto levantadas por profissionais de saúde, consumidores, patrocinadores de medicamentos ou escritórios de advocacia, a OPDP concede aos patrocinadores um prazo de trinta (30) dias corridos para responder.
Definição de material promocional
A expressão «material promocional» refere-se a rótulos promocionais e materiais publicitários, independentemente do formato, forma ou meio através do qual são comunicados. A FDA supervisiona FDA dois (02) tipos de rotulagem para medicamentos:
- Rotulagem FDA
- Etiquetagem promocional
De acordo com a secção 201(m) FDA, a rotulagem é definida como «todos os rótulos, além dos escritos, impressos ou gravados em relevo em qualquer recipiente, embalagem ou em qualquer artigo ou que acompanhe tal artigo». A linguagem utilizada em «que acompanhe tal artigo» é considerada uma interpretação ou explicação do material promocional, conforme declarado pelo US Tribunal US .
Critérios para a apresentação de material promocional para análise
- Inclusão dos BLA NDA, ANDA ou BLA adequados
- Nos casos em que os requerentes necessitem de uma análise imediata, enviar os pedidos ao gestor de projeto OPDP
- A partir do formulário FDA , atribua o tipo de material mais específico para representar o material promocional.
- Os diferentes tipos de materiais devem ser apresentados separadamente
- Não misturar outros envios com material promocional
- O material promocional dirigido aos profissionais de saúde deve ser apresentado separadamente do material dirigido aos consumidores
As métricas abaixo clarificam o número de formulários 2253 apresentados e os materiais incluídos nesses formulários.
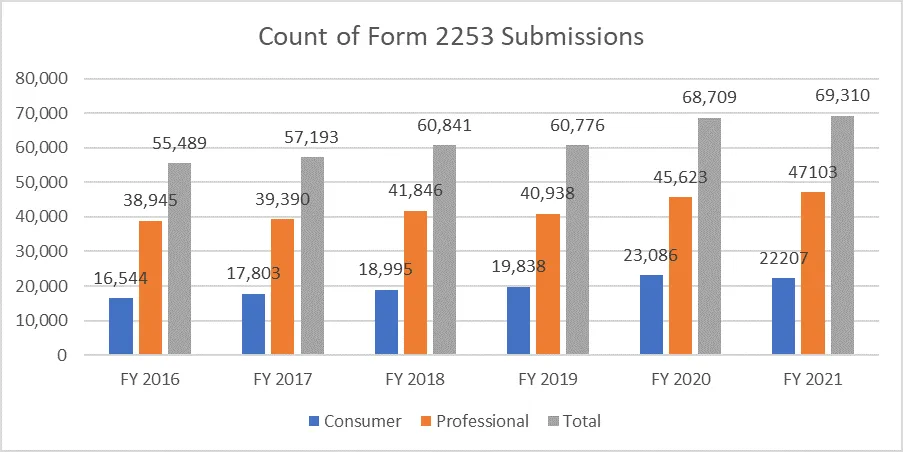
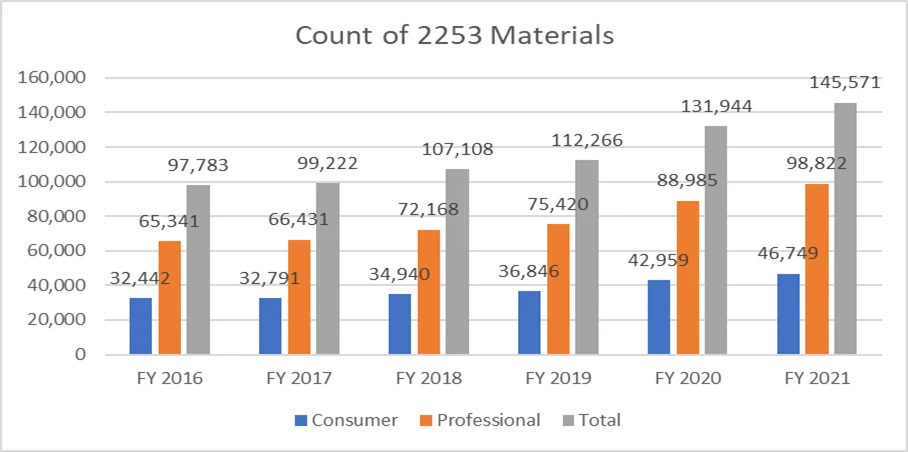
É de extrema importância que os patrocinadores elaborem o seu material promocional de acordo com as orientações fornecidas pela FDA evitar múltiplos ciclos de revisão, dado o custo do processo. Ter recursos que possam ajudar a facilitar o processo de envio de material promocional de forma integrada pode permitir que os patrocinadores alcancem os seus objetivos comerciais e permaneçam em conformidade com os requisitos regulamentares. Um parceiro regulatório comprovado como Freyr garantir uma revisão completa do material promocional e não promocional antes do envio, seja em formato eletrónico ou não eletrónico. Entre em contacto com Freyr hoje mesmo para elaborar material promocional claro, conciso e em conformidade com as normas desde a primeira vez.









