In der sich ständig weiterentwickelnden Landschaft der pharmazeutischen Entwicklung ist der Weg von der Entdeckung im Labor bis zur Behandlung des Patienten mit komplexen regulatorischen Herausforderungen gepflastert. In diesem Prozess liegt die Zulassungsantragstellung für neue Arzneimittel (NDA), ein wichtiger Meilenstein, der wissenschaftliche Anstrengungen und Investitionen umfasst. Dieser Blog befasst sich mit den Feinheiten der NDA und bietet wertvolle Einblicke und Erkenntnisse von Branchenveteranen.
Die NDA
Zulassungsanträge für neue Arzneimittel sind das Ergebnis umfangreicher Forschungs-, Entwicklungs- und klinischer Testarbeiten. Sie dienen als umfassende Unterlagen, die Aufsichtsbehörden wie die US-amerikanische Food and Drug Administration (FDA) davon überzeugen, dass ein neues Arzneimittel sicher und wirksam ist und für die Marktzulassung bereit ist.
Die Komplexität des NDA
Eine der größten Hürden bei NDA ist die schiere Menge und Komplexität der erforderlichen Daten. Pharmaunternehmen müssen sich durch ein Labyrinth von behördlichen Richtlinien kämpfen und gleichzeitig klare, überzeugende Beweise für die Vorzüge ihres Arzneimittels vorlegen. Dieser Balanceakt führt oft zu Verzögerungen, kostspieligen Überarbeitungen und in einigen Fällen sogar zu vollständigen Ablehnungen.
Um diesen wichtigen Prozess zu beleuchten, wollen wir die wichtigsten Phasen der NDA aufschlüsseln und Strategien für den Erfolg in jeder Phase untersuchen.
Tabelle 1: Wichtige Etappen bei NDA
| Bühne | Beschreibung | Bewährte Praktiken |
|---|---|---|
| Präklinische Forschung | Labor- und Tierstudien zur Sammlung erster Daten | Gewährleistung eines soliden Studiendesigns und einer sorgfältigen Datenerfassung |
| Klinische Studien | Versuche am Menschen in Phasen (I, II, III) | Umsetzung strenger Protokolle und Wahrung der Datenintegrität |
| Dokumentation | Zusammenstellung von Daten zur Sicherheit, Wirksamkeit und Qualität | Daten systematisch zu organisieren und für eine klare Darstellung zu sorgen |
| Regulatorische Überprüfung | Einreichung bei FDA Überprüfungsprozess | Aufrechterhaltung einer offenen Kommunikation mit den Regulierungsbehörden |
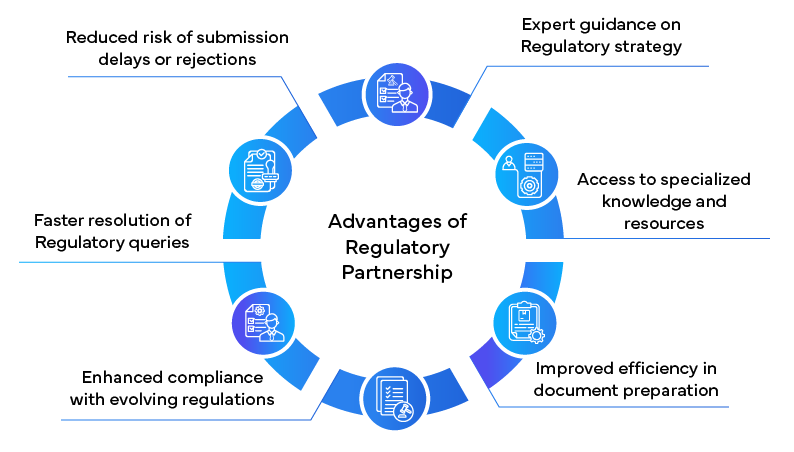
Die Rolle der regulatorischen Partnerschaft
Bei der Navigation durch die komplexe NDA wenden sich viele Pharmaunternehmen an Partner im Bereich Regulatory Affairs, um Unterstützung zu erhalten. Diese spezialisierten Unternehmen bieten einen reichen Erfahrungsschatz und Fachwissen, wodurch der NDA erheblich optimiert werden kann.
Gelernte Lektionen
Mit Blick auf die Zukunft wird die Bedeutung effektiver NDA weiter zunehmen. Angesichts des sich beschleunigenden Innovationstempos und der sich wandelnden regulatorischen Rahmenbedingungen werden diejenigen, die diesen kritischen Prozess beherrschen, am besten in der Lage sein, Patienten auf der ganzen Welt lebensverändernde Therapien anzubieten.
Der Weg zu einer erfolgreichen NDA ist selten einfach. Durch einen strategischen Ansatz bei regulatorischen Vorgängen, die Nutzung von Partnerschaften mit Experten und die konsequente Einhaltung von Qualitäts- und Compliance-Standards können Pharmaunternehmen ihre Chancen auf NDA jedoch erheblich verbessern.