SOP und SOP - Überblick
Die Biowissenschaftsbranche bewegt sich in Richtung Standardisierung von Verfahren, risikobasierte Methodik, Quality by DesignQbD) und einen gemeinsamen Kontrollrahmen. Die Überprüfung von StandardarbeitsanweisungenSOP) und die Erstellung von SOP erfordern jedoch manchmal, dass Unternehmen Zeit und Geld investieren, um die globale Gesetzgebung zu erforschen und die Systeme immer wieder zu aktualisieren. In solchen Fällen suchen Unternehmen nach Experten für das Schreiben von SOP und die Überprüfung von SOP .
Freyr bietet SOP für alle Arten von pharmazeutischen Verfahren, Forschung und Entwicklung, Annual Product Quality Review (APQR), Informationstechnologie, Regulatory Affairs, Quality Management Review, klinische Forschung und alle Kategorien von pharmazeutischen SOPs.
Mit umfassenden Kenntnissen im Verfassen neuerSOP oder im Ändern/Standardisieren bestehender SOPs bietet unser Team end-to-end DienstleistungenSOP und SOP , die folgende Bereiche abdecken:
SOP | SOP | SOP |
|
|
|
Freyr bietet einen integrierten Prozess mit mehreren Managementsystemen (ISO 9001, ISO 27001 mit USFDA, EMEA und MHLW) | ||
SOP
SOP
Freyr bietet Dienstleistungen zur Erstellung von SOP und zur Überprüfung von SOP für die Pharma-, Gesundheits- und Biotechnologiebranche an. In den letzten fünf (05) Jahren hat das Kompetenzzentrum für Compliance, Audit & ValidierungCoE) von Freyrmehr als fünftausendfünfhundert (5500) SOPs für seine Kunden erstellt/überprüft/harmonisiert und unterstützt sie weiterhin.
Auf der Grundlage eines risikobasierten Ansatzes und gemeinsamer Kontrollrahmenmethoden unterstützen wir Organisationen mit integrierten SOPs, die alle gesetzlichen Anforderungen erfüllen. Unsere QMS-Sanierungsexperten können eine Prozessarchitektur durch Integration mehrerer Vorschriften für einheitliche Managementsysteme einrichten (ISO 9001, ISO 27001, GLP - 17025, Medizinische Laboratorien - 15189, CAP mit USFDA, EMEA, MHLW, WHO, GxP und ICH).

- Prozessgestaltung
- Aufbau einer Prozessarchitektur
- Risikobasierter Ansatz
- Gemeinsamer Kontrollrahmen
- Integration mehrerer Vorschriften für einheitliche Verwaltungssysteme
Darüber hinaus hat Freyr mehr als zwanzig (20) große, mittlere und kleine Pharmaunternehmen bei der Vorbereitung auf Audits (einschließlich SOP ) durch globale Gesundheitsbehörden (HAs) unterstützt, darunter die US FDA, MHRA, EMA, CDSCO, ANVISA, SFDA, HALMED, NPRA, HSA und Health Canada.
Prozessansatz für die Aktualisierung und Erstellung von SOPs
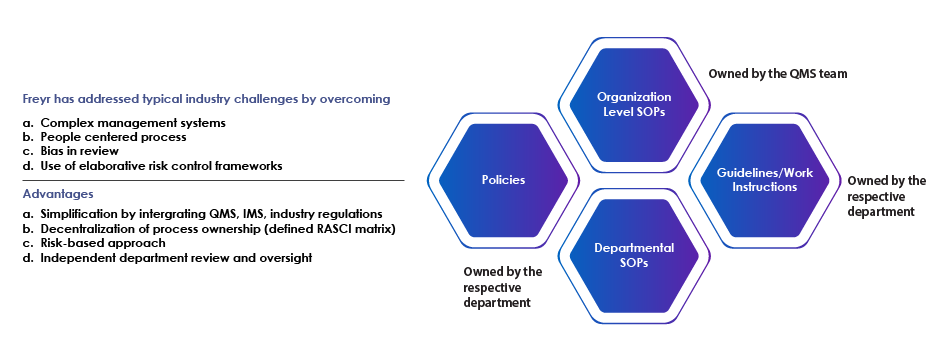
Erstellung und Überprüfung von SOP
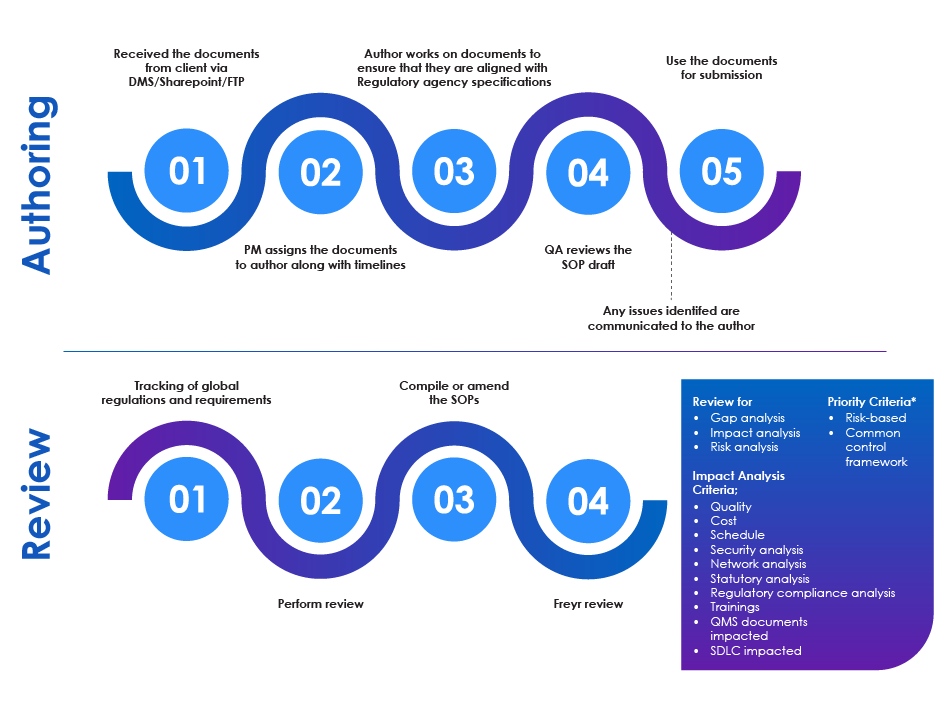
Überprüfung und Abzeichnung durch den Kunden
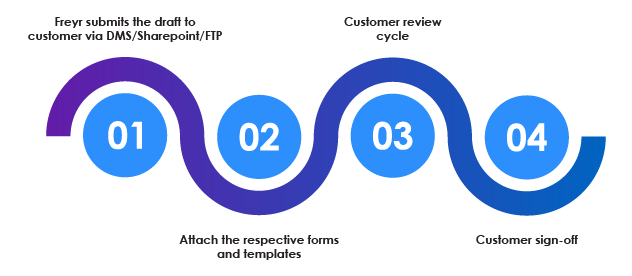
Überblick über die Abteilung SOP Writing
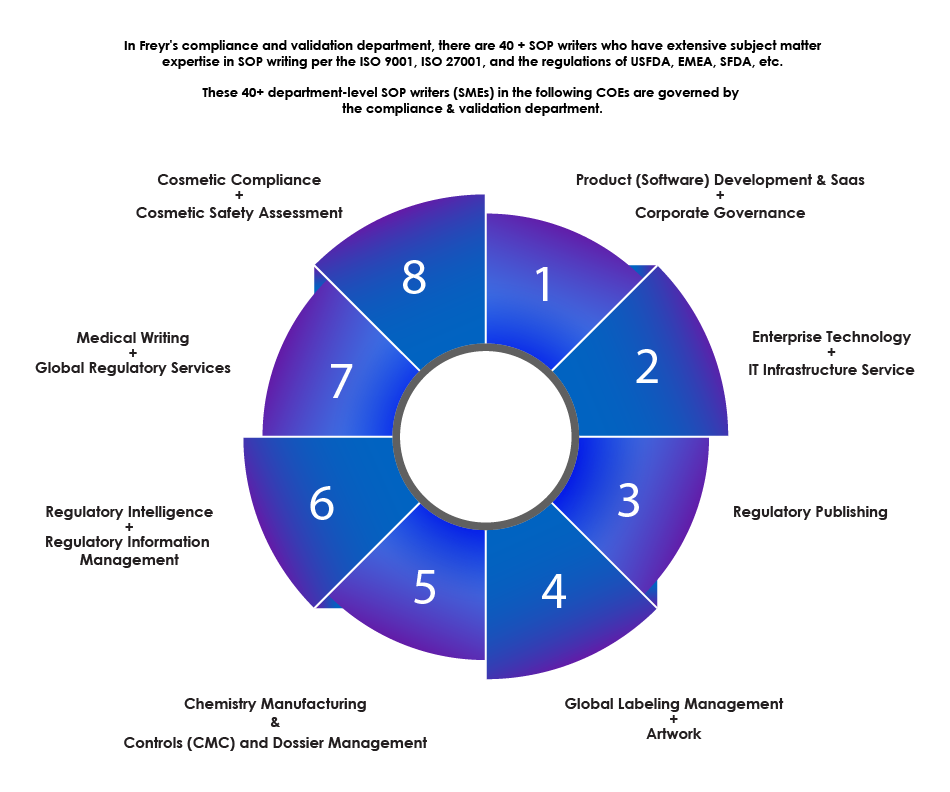
Freyr's Expertise in der Erstellung von SOP

SOP
Bei der Ausweitung von Geschäften auf neue Märkte müssen Life-Sciences-Unternehmen neue SOPs auf der Grundlage der regionalen gesetzlichen Anforderungen entwickeln oder die bestehenden Prozesse aktualisieren/verbessern, um sie an die neuen Anforderungen anzupassen. Vor der Erstellung von SOP sollten jedoch die Lücken zwischen den Prozessen identifiziert und entsprechend beseitigt werden.
Freyr hat Erfahrung mit einer Reihe von Projekten zur SOP . Der einfachste Teil des Dienstleistungsangebots ist die Überprüfung bestehender SOPs auf Genauigkeit und die Erstellung von Lückenanalyseberichten, bis hin zu komplexen Projekten, die eine SOP und -Sanierung beinhalten und zu einer SOP , Rationalisierung oder SOP führen.
SOP
Mit dem Wachstum des Unternehmens steigen auch die zu befolgenden oder einzuhaltenden Normen. Es kommt vor, dass ein Kunde mehrere Normen und Vorschriften zu befolgen hat, zu denen auch die SOPs für die Sicherheit in der pharmazeutischen Industrie gehören können. In solchen Szenarien verdoppelt sich die Komplexität der Verfahren für die Unternehmen, wenn sie für jeden Standard verschiedene SOPs pflegen und befolgen müssen. Das Gebot der Stunde ist es, die SOPs zu standardisieren.
SOP
Manchmal erstellen Organisationen SOPs, um die Prüfung loszuwerden. Aber es ist sinnlos, diese zu implementieren. Entweder werden sie von den Mitarbeitern nicht befolgt, oder sie könnten die Prozesse kompliziert machen, wenn sie integriert werden. Um solche Situationen zu vermeiden, ist es notwendig, die SOPs zu rationalisieren, die einen gewissen Wert für die Organisation haben.
Freyr bietet Dienstleistungen zur Überprüfung und Rationalisierung von SOP unter Einhaltung der geltenden Vorschriften an und unterstützt Organisationen bei der erfolgreichen Durchführung von SOP , was einen echten Mehrwert für das Unternehmen darstellt.
SOP und SOP
Obwohl es keine Leitlinien gibt, müssen die Standardarbeitsanweisungen generell in festgelegten und regelmäßigen Abständen überprüft werden. Da sich verschiedene Formate und Versionen angesammelt haben, besteht immer die Möglichkeit von Überschneidungen und Doppelarbeit. In solchen Zeiten müssen Organisationen ihre SOPs abstimmen und gleichzeitig die Prozesse kontinuierlich verbessern, um ihr Wachstum und ihre Geschäftstätigkeit zu unterstützen.
Mit seinem Wissen über SOPs und Qualitätssysteme unterstützt Freyr Unternehmen dabei, die SOPs regelmäßig abzustimmen und zu optimieren. Unser Expertenteam für Compliance kann schrittweise Aktualisierungen überwachen und durchführen.
SOP
Fusionen und Übernahmen sind ein fester Bestandteil des heutigen Geschäftsszenarios. Aber wenn sie stattfinden, kann die Zusammenführung und Verwaltung der Verfahren, Standards, SOPs und Qualitätssysteme beider Organisationen zermürbend sein. Neben der Anpassung an die bestehenden Standards kann die Erstellung von SOPs für die neu gegründete Organisation sogar noch hektischer sein, insbesondere bei kurzen Fristen.
Mit einem internen Compliance-Team Freyr end-to-end SOP Freyr , um die Lücken zwischen den Systemen beider Organisationen zu analysieren, bestehende Systeme zu standardisieren und bei Bedarf neue SOPs zu entwerfen. Unsere Experten erweitern die Unterstützung bei der Systemintegration um die Gestaltung nahtloser Prozesse und Arbeitsabläufe.
- Vorschläge für kosteneffiziente Prozessoptionen, ohne das Ziel der Produktqualität, der Einhaltung gesetzlicher Vorschriften, der Patientensicherheit, der Datenintegrität und der Sicherheit zu gefährden
- Integrierte Prozessmodelle
- Bewährte und praktikable Validierungs- und Qualifizierungsstrategien
- Schnelle Abwicklungszeit





