As pesquisas e os avanços modernos mudaram a dinâmica do panorama das ciências da vida. Os governos e as autoridades sanitárias enfrentam constantemente novos desafios em meio à mudança de paradigma da era pré-COVID era o cenário atual. Esse ambiente desafiador provocou uma end-to-end do setor, desde o desenvolvimento de novos medicamentos até a gestão da cadeia de abastecimento. Os esforços acelerados no desenvolvimento, implantação e distribuição da vacina contra a COVID-19 orquestraram uma frente unida contra a pandemia.
Dado que a procura de vacinação em todos os continentes continua a aumentar exponencialmente, o principal obstáculo que envolve capacidades de produção limitadas conduz ainda mais à escassez de vacinas e a atrasos no fornecimento. Esta escassez afecta as campanhas de vacinação em massa nos países. Para resolver o problema, a oferta tem de aumentar a par da procura. As autoridades reguladoras de todo o mundo devem desenvolver uma estrutura eficaz e adaptada às necessidades específicas de cada país. Com uma tal diversidade de dados de eficácia e segurança, os documentos e os requisitos parecem variar de país para país. Por exemplo, a consolidação dos requisitos documentais e a aceleração da aprovação regulamentar dos módulos desempenharam um papel muito significativo na entrega rápida de vacinas à massa numa questão de oito (08) meses para introduzir o primeiro produto no mercado.
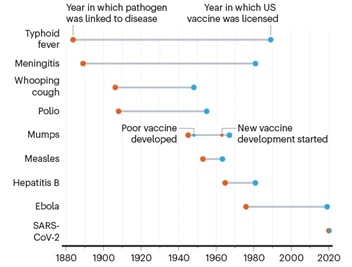
As vacinas contra a COVID-19 são o epítome da excelência científica e regulatória. Ao minimizar a estrutura multicamadas para documentação sem módulos repetitivos, o processo de autorização torna-se mais estruturado, eliminando atrasos na entrada no mercado em regiões carentes de abastecimento. Em 2017, foi realizada uma análise para comparar os procedimentos de registo específicos para produtos vacinais em 134 países. Em conclusão, a diferença percentual foi quase três (03) vezes maior do que a semelhança percentual quando comparada com o ICH proposto para nações internacionalmente. Isso por si só demonstra a natureza fragmentada dos requisitos regulatórios com autorizações em níveis regionais.
Ao explorar o acesso ao mercado nos países em desenvolvimento, nenhuma abordagem padrão parece ser suficiente. Uma abordagem multifacetada que envolva a identificação de indicadores qualitativos e quantitativos para a população local, as capacidades dos pagadores e as oportunidades de financiamento pode alimentar a tomada de decisões. No que respeita aos mercados emergentes a nível mundial, quase 18% do total dos mercados estão bem representados por produtos de vacinas, avaliados em mais de 24 mil milhões de dólares. Os investigadores acreditam que estes factos podem ser apenas uma subavaliação do que existe. Por conseguinte, identificar mercados e explorar o potencial de mercado pode ser o próximo passo para si.
Procura um parceiro que só se contenta com a excelência? Consulte Freyr.
Manter-se informado. Mantenha-se atualizado.









