
Nos últimos tempos, o aparecimento de impurezas de nitrosaminas em certas substâncias de medicamentos genéricos levou a uma reavaliação das práticas da indústria. Este blogue dá um mergulho profundo no mundo multifacetado da atenuação das nitrosaminas, especificamente no contexto dos medicamentos genéricos. Além disso, também lança luz sobre as considerações feitas para as impurezas relacionadas com a substância medicamentosa nitrosamina. Exploramos os meandros da manutenção da qualidade, garantindo a bioequivalência e compreendendo o papel fundamental dos especialistas em regulamentação neste processo crítico.
O desafio das nitrosaminas: Um apelo à ação regulamentar
As nitrosaminas, uma classe de compostos conhecidos por serem potenciais carcinógenos, apresentam um desafio regulatório complexo. Agências reguladoras, incluindo a FDA dos EUA FDA a Agência Europeia de Medicamentos (EMA), responderam com limites e diretrizes rigorosos para a presença dessas impurezas em produtos farmacêuticos. Isso requer uma abordagem abrangente para compreender, detectar e mitigar o risco de impurezas de nitrosamina em medicamentos genéricos.
Desafios da bioequivalência em produtos genéricos: Equilíbrio entre segurança e equivalência
A bioequivalência é a pedra angular do desenvolvimento de medicamentos genéricos, garantindo que um produto genérico é terapeuticamente equivalente ao seu homólogo de referência. Este aspeto crítico torna-se ainda mais complexo no contexto da atenuação das impurezas relacionadas com as nitrosaminas.
1. Assegurar a coerência da formulação
A presença de impurezas de nitrosamina depende da entrega consistente do ingrediente farmacêutico ativo (API) ao doente. Os especialistas em regulamentação, em colaboração com os cientistas da formulação, desempenham um papel fundamental na garantia de que quaisquer ajustes efectuados para atenuar as impurezas não comprometem a estabilidade ou a eficácia da formulação.
2. Impactos na absorção e na farmacocinética
As impurezas de nitrosaminas podem potencialmente afetar a absorção e a farmacocinética do medicamento. Isto é particularmente preocupante no contexto dos produtos genéricos, onde variações subtis podem ter efeitos pronunciados. Os especialistas em regulamentação orientam estes estudos para garantir que cumprem as normas regulamentares e fornecem informações significativas sobre a segurança e a eficácia do produto genérico.
3. Estudos de dissolução: Um componente-chave
As impurezas de nitrosamina podem influenciar as taxas de dissolução, e os especialistas em regulamentação trabalham em estreita colaboração com as equipas de formulação e análise para desenvolver e implementar métodos de teste de dissolução robustos. Estes métodos devem ser suficientemente sensíveis para detetar variações nos perfis de dissolução que possam surgir devido à presença de impurezas.
4. Controlo e vigilância pós-aprovação
Mesmo após a aprovação regulamentar, o monitoramento de produtos genéricos quanto à presença de impurezas de nitrosamina continua. Estudos pós-aprovação e esforços de farmacovigilância são liderados por especialistas regulamentares que trabalham em colaboração com os fabricantes para implementar programas de monitoramento robustos. Essa vigilância contínua é crucial para identificar e resolver prontamente quaisquer preocupações de segurança emergentes associadas a impurezas de nitrosamina.
O papel dos peritos em matéria de regulamentação: Navegar no cenário complexo
Assuntos Regulamentares desempenham um papel fundamental na mitigação dos desafios impostos pelas impurezas relacionadas com nitrosaminas em medicamentos genéricos. As suas responsabilidades multifacetadas abrangem vários domínios e estão representadas no gráfico circular abaixo:
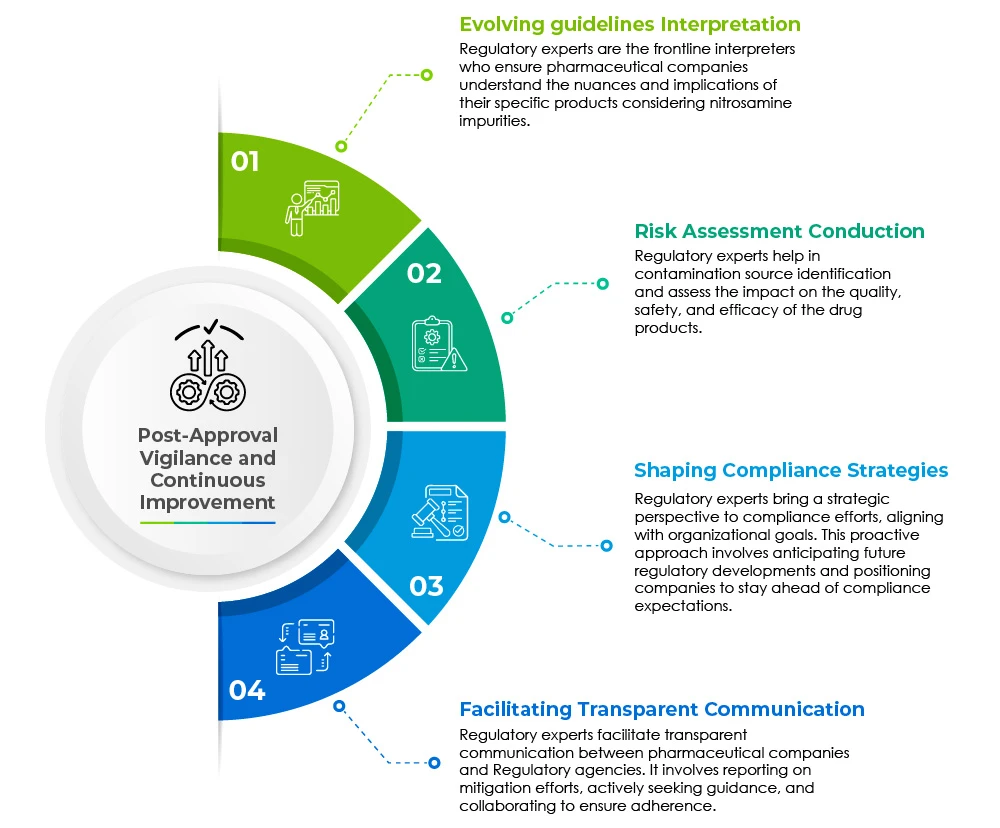
A vigilância pós-aprovação e a melhoria contínua são as pedras angulares para uma assistência regulamentar rápida.
Conclusão: Salvaguardar a saúde pública através da vigilância e do conhecimento especializado
Mitigar as impurezas relacionadas com nitrosaminas não é apenas um requisito regulamentar; é um compromisso com a saúde pública. À medida que a indústria farmacêutica enfrenta este desafio, o papel dos especialistas em regulamentação torna-se fundamental. A sua capacidade de combinar conformidade com inovação garante que os medicamentos genéricos não só cumpram as normas regulamentares, mas também contribuam para um futuro mais seguro e saudável. Na Freyr, os nossos especialistas em regulamentação aproveitam os seus conhecimentos para obter uma vantagem competitiva nessas atividades para as empresas farmacêuticas. us para saber mais.









