
Introdução
A Direção Europeia para a Qualidade dos Medicamentos e Cuidados de Saúde anunciou recentemente uma atualização do seu processo (CEP), que promete ser mais eficiente, transparente e fácil de utilizar do que o seu antecessor. Neste blogue, vamos explorar as vantagens e o papel dos fornecedores de serviços de regulamentação para ajudar as empresas farmacêuticas a navegar neste novo sistema.
CEP 2.0: CEP do futuro
A atual garantia da qualidade e segurança dos Medicamentos. No entanto, a falta de harmonização no cumprimento dos requisitos do CEP em diferentes regiões e a ineficiência no processo deram início à atualização. Por exemplo, houve casos em que as empresas enviaram os documentos e esperaram vários meses sem qualquer feedback. Como resultado, o processo tornou-se demorado e opaco para as partes interessadas.
O CEP 2.0 abordou estes desafios em todo o sistema. De acordo com a EDQM, esta versão do CEP garante um processo mais simplificado e eficiente, com maior transparência entre as partes interessadas.
Alterações em
O CEP 2.0 apresenta várias mudanças no processo. Algumas delas são as seguintes:
A. Processo totalmente digital: esta alteração indica que as empresas farmacêuticas deixarão de ser obrigadas a fornecer cópias impressas dos seus submissão CEP. Em vez disso, poderão submeter as suas candidaturas por via eletrónica através do portal de submissão CEP da EDQM.
B. Introdução de uma online : permite às empresas acompanhar o andamento dos seus pedidos em tempo real. Também fornece acesso a todas as comunicações entre a EDQM e o requerente, incluindo quaisquer questões ou preocupações levantadas durante o processo de análise.
C. Fase pré-apresentação: ajuda os requerentes a identificar quaisquer questões ou preocupações relacionadas com submissão sua submissão CEP submissão a enviar para análise. O requerente pode apresentar um pedido de informação pré-apresentação, que será analisado pela EDQM no prazo de vinte (20) dias úteis. A EDQM fornecerá feedback sobre a adequação submissão CEP e identificará quaisquer questões potenciais a serem abordadas pelo requerente.
As alterações relacionadas com a implementação são destacadas na infografia abaixo:
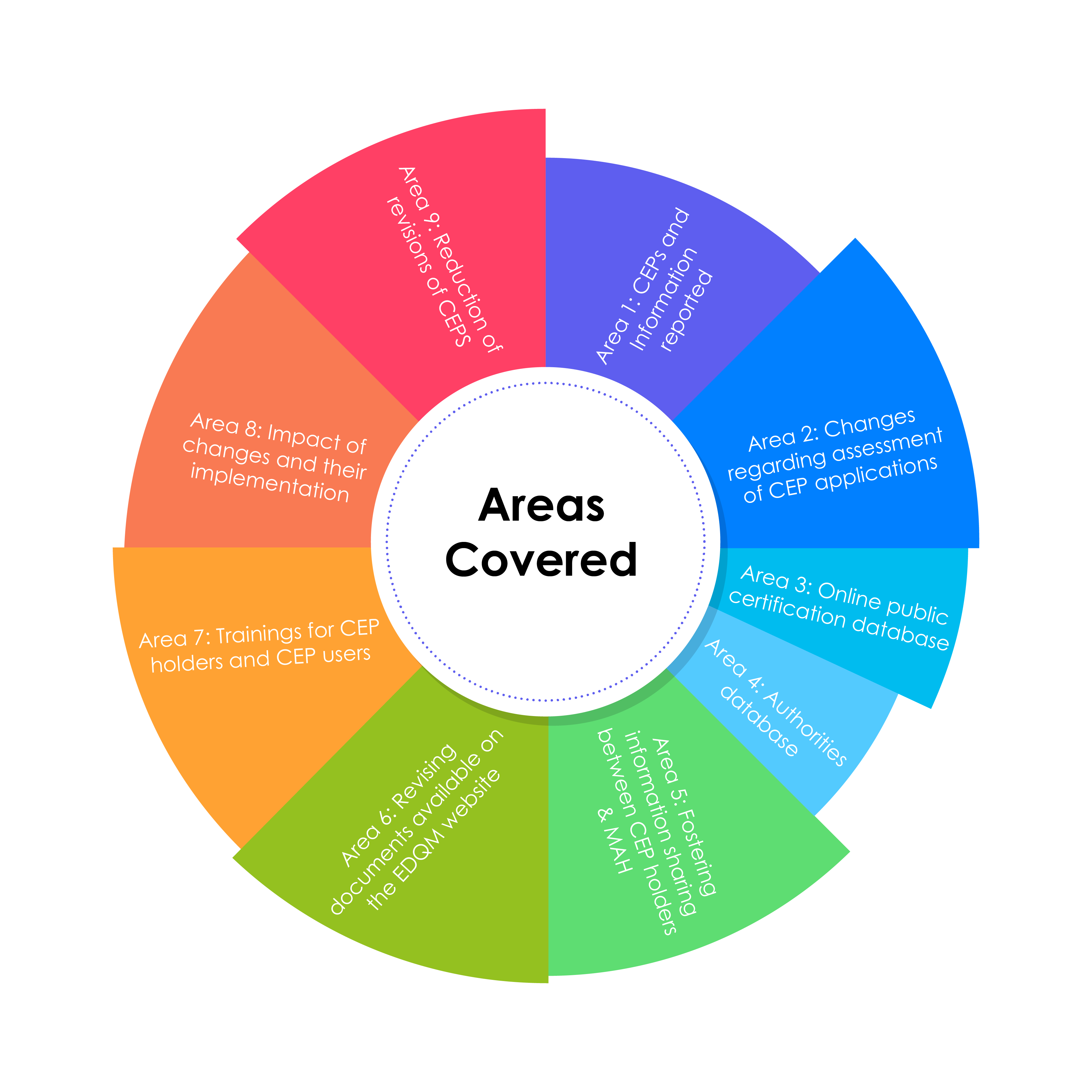
Áreas abrangidas pelo CEP 2.0 da EDQM: O CEP do Futuro
Desafios no processo de certificação
O novo processo coloca desafios significativos aos fabricantes de produtos farmacêuticos que procuram a certificação. Navegar pelas complexidades do processo requer conhecimentos especializados e experiência que muitas empresas podem não ter. Alguns dos desafios são:
- Pré-requisito de especialização: O CEP 2.0 introduz um processo totalmente digital submissão revisão do CEP do candidato, o que exigirá um especialista em sistemas.
- Obrigação de eficiência: O novo sistema apresentará um processo de avaliação simplificado, o que reduzirá o tempo que a EDQM leva a avaliar os pedidos de CEP e a emitir certificados. Isto desafia as empresas farmacêuticas a terem um sistema eficiente para cumprir os requisitos.
- Exigência de conformidade: Os processos do CEP 2.0 garantem que as empresas farmacêuticas cumpram todos os regulamentos relacionados. Por outro lado, as empresas farmacêuticas precisam de compreender os requisitos de conformidade relativos a novas medidas de proteção de dados, normas de apresentação de informações e regulamentos recentemente introduzidos.
Nesses esforços, os fornecedores de regulamentação podem desempenhar um papel vital para ajudar os fabricantes a navegar no novo processo. A parceria com fornecedores regulamentares experientes pode ajudar a garantir um resultado bem-sucedido através da aprovação atempada dos CEPs.
O CEP 2.0 promete ser uma grande mudança para as empresas farmacêuticas que desejam entrar no mercado da UE. O novo sistema oferece várias vantagens em relação ao seu antecessor, incluindo uma submissão simplificada submissão processo CEP, um processo de avaliação otimizado, maior transparência e medidas de proteção de dados aprimoradas. Os fornecedores regulatórios podem desempenhar um papel fundamental em ajudar as empresas farmacêuticas a navegar neste novo sistema, fornecendo experiência, eficiência e orientação em conformidade.
Na Freyr, a nossa equipa pode garantir que a compilação, revisão e envio do CEP sejam feitos sem complicações. O parceiro regulatório certo para o envio do CEP pode conduzir a sua organização através de quaisquer obstáculos, rumo a uma jornada infalível e em conformidade. Consulte Freyr para saber mais sobre a nossa experiência.









