
Die Etiketten von Arzneimitteln dienen den Anwendern als Leitfaden aus erster Hand und helfen bei der qualitativen Verwendung der Produkte. Daher ist es äußerst wichtig, dass die Informationen auf den Etiketten konsistent, leicht lesbar und fehlerfrei sind und den globalen Standards entsprechen. Um dies zu erreichen, hat die Therapeutic Goods Administration (TGA) einige Änderungen an der Art und Weise vorgenommen, wie die Informationen auf den Etiketten der Produkte dargestellt werden. Ziel dieser Änderungen ist es, die Klarheit und Konsistenz der Informationen für das medizinische Fachpersonal zu verbessern.
Was sind die neuen Änderungen am Etikett?
Obwohl die neuen Informationen bereits berücksichtigt und von den Herstellern umgesetzt wurden, ist es ratsam, sie für eine umfassende Darstellung im Detail zu kennen. Nachfolgend sind einige von ihnen aufgeführt, die die Hersteller bei der Gestaltung ihrer Arzneimittelkennzeichnungen berücksichtigen müssen.
1. Informationen zum Wirkstoff
Nach der neuen Vorschrift sollten aktive Inhaltsstoffe sein:
- Deutlichere Platzierung auf der Vorderseite der Arzneimittelpackung
- Sollte unter oder neben dem Namen des Arzneimittels auf der Vorderseite der Arzneimittelpackung stehen
- Sie müssen leicht zwischen den Arzneimitteln vergleichbar sein.
2. Medizinische Informationen
Um sicherzustellen, dass Anwender und Angehörige der Gesundheitsberufe eine fundierte Entscheidung treffen, sollten die Arzneimittelinformationen klarer formuliert sein:
- Kritische Gesundheitsinformationen in unverwechselbaren Etiketten
- Alle obligatorischen Angaben müssen sich klarer und deutlicher von der Hintergrundfarbe abheben, damit sie besser lesbar sind.
- Meldepflichtige Stoffe, wie Allergene, müssen auf dem Etikett angegeben werden.
3. Kritische Gesundheitsinformationen
Die kritischen Gesundheitsinformationen helfen dem Verbraucher bei der sicheren Anwendung des Arzneimittels, indem sie wichtige Informationen liefern. Die Informationen in der Tabelle mit den kritischen Gesundheitsinformationen sind immer in der gleichen Reihenfolge aufgeführt, auch wenn die Darstellung der Informationen leicht abweichen kann. Die kritischen Gesundheitsinformationen haben die folgenden Überschriften und Informationen in der gleichen Reihenfolge:
- Aktive Bestandteile: Name des Wirkstoffs und seine Menge
- Indikationen: Verwendung des Arzneimittels
- Warnhinweise: Enthält Warnhinweise, Ratschläge und zusätzliche Warnungen zur Verwendung des Arzneimittels unter 'Gebrauchsanweisung'.
- Gebrauchsanweisung: Enthält Informationen über die sichere Anwendung des Medikaments
- Sonstige Informationen: Enthält Informationen wie Angaben zur Aufbewahrung, Sicherheitsmerkmale, Kontaktangaben zum Sponsor, Liste der Inhaltsstoffe usw. Dieser Teil erscheint möglicherweise nicht auf jedem Arzneimittel
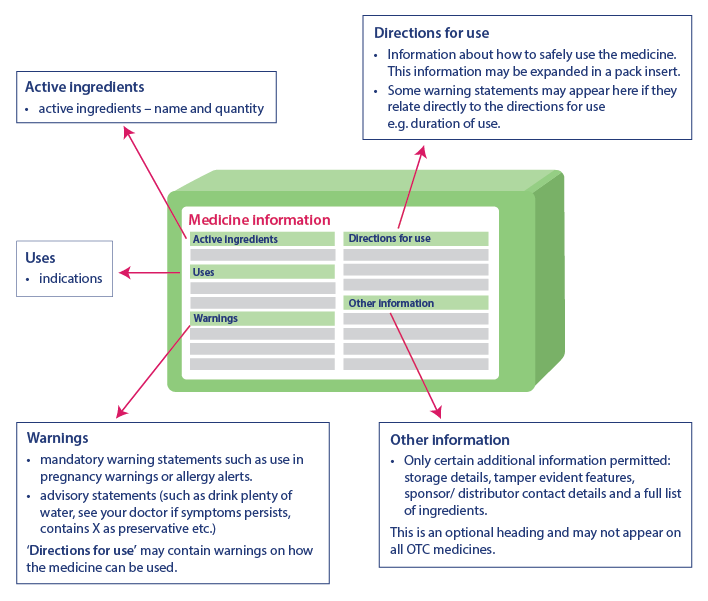
Quelle: TGA
4. Abgabe in der Apotheke
Nach der neuen Vorschrift werden folgende Änderungen an den Arzneimittelspendern vorgenommen:
- Um die Identifizierung der Medikamente zu verbessern, müssen die Kartons der verschreibungspflichtigen Medikamente auf den drei nicht gegenüberliegenden Seiten ihren Namen tragen
- Die Etiketten von verschreibungspflichtigen Arzneimitteln müssen eine Fläche von 70x30 Millimetern haben, es sei denn, sie werden in einer Primär- oder Startpackung geliefert.
5. Informationen über Allergene
Auf den Etiketten von Arzneimitteln müssen die folgenden Informationen angegeben werden:
- Falls in dem Arzneimittel vorhanden, müssen alle Stoffe auf dem Etikett angegeben werden
- Weitere Stoffe wie Krustentiere, Fisch, Eier, Soja, Milch und Nüsse müssen auf dem Etikett angegeben werden.
- Im Falle neuer Allergene dürfen die Hersteller diese erst nach Ablauf der vierjährigen Übergangsfrist in die Liste aufnehmen.
Obwohl die TGA diese Informationen für Angehörige der Gesundheitsberufe veröffentlicht hat, halten wir es für eine wichtige Voraussetzung, dass auch die Hersteller ihre Produkte umfassend kennzeichnen. Auf diese Weise können die Angehörigen der Gesundheitsberufe die aktualisierten Informationen ohne Verwirrung einsehen und die Patienten zum sicheren Konsum anleiten. Bekanntlich hat die TGA den Herstellern eine Übergangsfrist von vier Jahren für die Umsetzung dieser Änderungen eingeräumt. Nach Ablauf dieser Frist müssen die Medikamentenetiketten den neuen Kennzeichnungsanforderungen entsprechen. Bleiben Sie informiert. Bleiben Sie vorschriftsmäßig.









